题目内容
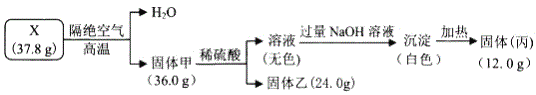
【题目】![]() 受热分解的化学方程式为:
受热分解的化学方程式为:![]() 。为检验
。为检验![]() 高温分解的产物,进行如下实验:
高温分解的产物,进行如下实验:
(1)检验产物![]() :少量
:少量![]() 高温分解得到的固体,加入一定量盐酸溶解,再向该溶液中加入适量的KSCN溶液,若有___现象产生,则证明产物中存在
高温分解得到的固体,加入一定量盐酸溶解,再向该溶液中加入适量的KSCN溶液,若有___现象产生,则证明产物中存在![]() 。
。
(2)检验气体产物:将![]() 高温分解产生的气体通入如图三个装置中,以检验产生的气体中是否含有
高温分解产生的气体通入如图三个装置中,以检验产生的气体中是否含有![]() 。
。
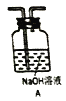
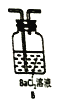
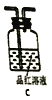
①三个装置的连接序为____(填装置序号);
②气体通过![]() 溶液时可以观察到白色沉淀现象,产生该现象的化学反应为_____(用一个化学反应方程式表示)
溶液时可以观察到白色沉淀现象,产生该现象的化学反应为_____(用一个化学反应方程式表示)
【答案】血红色 BAC BaCl2+SO3+H2O=2HCl+BaSO4↓
【解析】
(1)固体产物为Fe2O3中为三价铁,用盐酸使其溶解成溶液,Fe3+可使KSCN溶液会变血红色,所以加入一定量盐酸溶解,再向该溶液中加入适量的硫氰化钾溶液,若有血红色现象产生,则证明固体产物是Fe2O3;
答案为:血红色。
(2)①为防止二氧化硫被氧化成三氧化硫,应先检验三氧化硫在检验二氧化硫,故装置的连接顺序 应该为BAC;
答案为:BAC。
②气体通过![]() 溶液时,SO3溶于水生成硫酸,与氯化钡溶液能生成硫酸钡白色沉淀,发生反应的化学方程式为:BaCl2+SO3+H2O=2HCl+BaSO4↓。
溶液时,SO3溶于水生成硫酸,与氯化钡溶液能生成硫酸钡白色沉淀,发生反应的化学方程式为:BaCl2+SO3+H2O=2HCl+BaSO4↓。
答案为:BaCl2+SO3+H2O=2HCl+BaSO4↓。

练习册系列答案
相关题目