题目内容
【题目】反应C(s)+H2O(g)![]() CO(g)+H2(g)在一定容积的密闭容器中进行,则下列说法或结论中,能够成立的是( )
CO(g)+H2(g)在一定容积的密闭容器中进行,则下列说法或结论中,能够成立的是( )
A. 其他条件不变仅将容器的体积缩小一半,反应速率减小
B. 保持体积不变,充入少量He气体使体系压强增大,反应速率一定增大
C. 反应达平衡状态时:v(CO)正=v(H2O)逆
D. 其他条件不变,适当增加C(s)的质量会使反应速率增大
【答案】C
【解析】
A.其他条件不变仅将容器的体积缩小一半,物质的浓度增大,反应速率加快,A错误;
B.保持体积不变,充入少量He气体使体系压强增大,由于反应体系的物质浓度不变,所以反应速率不变,B错误;
C.反应达平衡状态时任何物质的浓度不变,用同一物质表示的反应速率相同,v(H2O)正=v(CO)正=v(H2O)逆,则v(H2O)正= v(H2O)逆,C正确;
D.其他条件不变,适当增加C(s)的质量,由于C是固体,物质的浓度不变,所以反应速率不变,D错误;
故合理选项是C。

 寒假天地重庆出版社系列答案
寒假天地重庆出版社系列答案【题目】草酸亚铁晶体(FeC2O4·xH2O)为淡黄色粉末,不溶于水,可作照相显影剂和制药工业,某化学兴趣小组对其性质进行如下探究。回答下列问题:
Ⅰ.定性探究
选用下列试剂设计实验方案,完成下表内容。
试剂:酸性KMnO4 溶液、H2O2 溶液、KSCN 溶液
操作 | 现象 | 结论与解释 |
(1)取少量草酸亚铁晶体于试管中,加入2mL 水,振荡后静 置 | 有淡黄色沉淀,上层清液无色 | ___________________________ |
(2)继续加入2mL稀硫酸,振荡 | 固体溶解,溶液变为浅绿色 | 草酸亚铁溶于硫酸,硫酸酸性____草酸(填“强于”、“弱于”或“等于”) |
(3)向步骤(2)所得溶液中滴加几滴K3[Fe(CN)6]溶液 | ___________ | 含有Fe2+ |
(4)________________________________ | ___________ | H2C2O4 或C2O42-具有还原性 |
Ⅱ.定量探究:滴定实验测x 的值
(5)滴定前,下列操作的正确顺序是c→ _________ →d(填字母序号)。
a.排尽滴定管尖嘴的气泡并调整液面 b.盛装0.1000 mol·L-1 的酸性KMnO4 溶液
c.查漏、清洗 d.初始读数、记录为0.50 mL
e.用0.1000 mol·L-1 的酸性KMnO4 溶液润洗
(6)称取 m 克样品,加入适量稀硫酸溶解,用步骤(5)准备的标准KMnO4 溶液直接滴定,溶解时最适合的玻璃仪器是_______________ ,滴定反应的氧化产物是________________。
(7)终点读数为20.50mL。结合上述实验数据求得x=____________(用含m 的代数式表示,FeC2O4 的相对分子质量为144)。
【题目】Ⅰ.羰基硫(COS)广泛存在于以煤为原料的各种化工原料气中,能引起催化剂中毒、化学产品质量下降和大气污染,研究其脱除方式意义重大。回答下列问题:
(1)COS 的分子结构与 CO2 相似,COS 的电子式为_____。
(2)已知:① CO(g)+H2O(g) ![]() H2(g)+CO2(g) ΔH1=-41.2 kJ·mol-1
H2(g)+CO2(g) ΔH1=-41.2 kJ·mol-1
② COS(g)+H2O(g) ![]() H2S(g)+CO2(g) ΔH2=-35.5 kJ·mol-1
H2S(g)+CO2(g) ΔH2=-35.5 kJ·mol-1
则氢气脱除 COS 生成 CO 和 H2S 的热化学方程式为________________________________。
II. 通常人们把拆开 1 mol 某化学键所吸收的能量看成该化学键的键能。键能的大小可用于估算化学反应的反应热(△H),化学反应的△H 等于反应中断裂旧化学键的键能之和与反应中形成新化学键的键能之和的差。工业上高纯硅可通过下列反应制取:
SiCl4(g) + 2H2(g) = Si(s) + 4HCl(g) △H = + 236 kJ/mol
键能 | Si—O | Si—Cl | H—H | H—Cl | Si—Si | Si—C |
(kJ·mol-1) | 460 | 360 | 436 | 431 | x | 347 |
表中 x=_____。
Ⅲ. “绿水青山就是金山银山”,利用原电池原理(6NO2 +8NH3 = 7N2+12H2O)可以处理氮的氧化物和NH3 尾气,装置原理图如图:
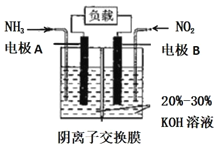
负极反应式为____________, 标准状况下有 4.48 L NO2 被处理时,转移电子的物质的量为_______mol。