题目内容
【题目】为探究矿物固体X(仅含4种短周期元素)的组成和性质,其中固体乙可制作光导纤维。现完成如下实验:
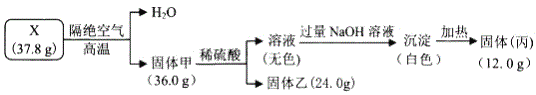
请回答:
(1)X的化学式为_____。
(2)X中所含的一种金属元素是___填元素符号),其单质在![]() 中燃烧的化学方程式为_____。
中燃烧的化学方程式为_____。
【答案】3MgO4SiO2H2O Mg 2Mg+CO2=C+2MgO
【解析】
固体乙可制光导纤维,应为SiO2,其物质的量为![]() =0.4mol,由表中数据可知生成水的质量为1.8g,物质的量为0.1mol,固体甲加入稀硫酸,得到无色溶液,加入过量的氢氧化钠溶液,得到白色沉淀,应为Mg(OH)2,加入生成丙为MgO,物质的量为
=0.4mol,由表中数据可知生成水的质量为1.8g,物质的量为0.1mol,固体甲加入稀硫酸,得到无色溶液,加入过量的氢氧化钠溶液,得到白色沉淀,应为Mg(OH)2,加入生成丙为MgO,物质的量为![]() =0.3mol,可知甲为3MgO4SiO2,则X为3MgO4SiO2H2O;
=0.3mol,可知甲为3MgO4SiO2,则X为3MgO4SiO2H2O;
(1)由分析知:X的化学式为3MgO4SiO2H2O;
答案为:3MgO4SiO2H2O。
(2)由以上分析可知X除了含有H、O元素以外还含有Mg、Si元素,其中Mg为金属元素,Mg单质在CO2中燃烧生成C和MgO,发生反应的化学方程式2Mg+CO2=C+2MgO;
答案为:Mg;2Mg+CO2=C+2MgO。

【题目】写出下列反应的化学(离子)方程式
(1)HF不能装在玻璃瓶中,对应发生的化学方程式________
(2)NO2与一定量的O2混合通入水中,完全被水吸收的离子方程式________
(3)Pb的常见化合价是+2价和+4价,PbO2的某些化学性质与MnO2相似。写出实验室用PbO2与浓盐酸混合加热制氯气的化学方程式________
(4)SO2气体使溴水褪色的离子方程式________
(5)煤燃烧排放的烟气含有SO2和NOx,形成酸雨、污染大气,采用NaClO2溶液作为吸收剂可同时对烟气进行脱硫、脱硝。回答下列问题:
在鼓泡反应器中通入含有SO2和NO的烟气,反应温度为323K,NaClO2溶液浓度为5×10-3mol·L-1.(溶液呈碱性)反应一段时间后溶液中离子浓度的分析结果如下表。
离子 | SO42- | SO32- | NO3- | NO2- | Cl= |
c/(mol·L-1) | 8.35×10-4 | 6.87×10-6 | 1.5×10-4 | 1.2×10-5 | 3.4×10-3 |
写出NaClO2溶液脱硝过程中主要反应的离子方程式 ________。