题目内容
下列离子方程式书写不正确的是( )
| A、NaHCO3溶液与过量的Ca(OH)2溶液反应:HCO3-+OH-+Ca2+=CaCO3↓+H2O |
| B、向1mol AlCl3溶液中加入2mol NaOH:Al3++4OH-=AlO2-+2H2O |
| C、铜片插入氯化铁溶液中:2Fe3++Cu=2Fe2++Cu2+ |
| D、少量CO2通入NaOH溶液中:CO2+2OH-=CO32-+H2O |
考点:离子方程式的书写
专题:离子反应专题
分析:A.二者反应是碳酸钙、氢氧化钠和水;
B.二者反应生成氢氧化铝和氯化钠;
C.二者反应生成氯化亚铁、氯化铜;
D.二者反应生成碳酸钠和水.
B.二者反应生成氢氧化铝和氯化钠;
C.二者反应生成氯化亚铁、氯化铜;
D.二者反应生成碳酸钠和水.
解答:
解:A.二者反应是碳酸钙、氢氧化钠和水,离子方程式为HCO3-+OH-+Ca2+=CaCO3↓+H2O,故A正确;
B.二者反应生成氢氧化铝和氯化钠,离子方程式为Al3++3OH-=Al(OH)3↓,故B错误;
C.二者反应生成氯化亚铁、氯化铜,离子方程式为2Fe3++Cu=2Fe2++Cu2+,故C正确;
D.二者反应生成碳酸钠和水,离子方程式为CO2+2OH-=CO32-+H2O,故D正确;
故选B.
B.二者反应生成氢氧化铝和氯化钠,离子方程式为Al3++3OH-=Al(OH)3↓,故B错误;
C.二者反应生成氯化亚铁、氯化铜,离子方程式为2Fe3++Cu=2Fe2++Cu2+,故C正确;
D.二者反应生成碳酸钠和水,离子方程式为CO2+2OH-=CO32-+H2O,故D正确;
故选B.
点评:本题考查了离子方程式正误判断,为高考热点,明确物质之间的反应是解本题关键,注意A、B、D离子方程式与反应物的量有关,为易错点.

练习册系列答案
相关题目
某溶液中由水电离产生的C(H+)=1×10-10mol/L,该溶液的溶质不可能是( )
| A、KOH |
| B、Na2CO3 |
| C、HClO4 |
| D、Na HSO4 |
下列有关金属的工业制法中,正确的是( )
| A、制钠:用海水为原料制得精盐,再电解纯净的NaCl溶液 |
| B、制铝:从铝土矿中获得氧化铝再得到氯化铝固体,电解熔融的氯化铝得到铝 |
| C、制镁:用海水为原料,经一系列过程制得氧化镁固体,H2还原得镁 |
| D、制铁:以铁矿石为原料,CO还原得铁 |
下列与含氯化合物有关的说法正确的是( )
| A、HClO是弱酸,所以NaClO是弱电解质 |
| B、向沸水中逐滴加入少量饱和FeCl3溶液,可制得Fe(OH)3胶体 |
| C、用加热的方法可以将NH4Cl与碘的混合物分离 |
| D、ClO-与Fe2+、H+均能大量共存 |
肼(N2H4)是火箭发动机的燃料,它与N2O4反应时,N2O4为氧化剂,生成氮气和水蒸气.已知:N2(g)+2O2(g)═N2O4(g)△H=+8.7kJ/mol,N2H4(g)+O2(g)═N2(g)+2H2O(g)△H=-534.0kJ/mol,下列表示肼跟N2O4反应的热化学方程式,正确的是( )
| A、2N2H4(g)+N2O4(g)═3N2(g)+4H2O(g)△H=-542.7kJ/mol |
| B、2N2H4(g)+N2O4(g)═3N2(g)+4H2O(g)△H=-1059.3kJ/mol |
| C、2N2H4(g)+N2O4(g)═3N2(g)+4H2O(g)△H=-1076.7kJ/mol |
| D、N2H4(g)+N2O4(g)═N2(g)+2H2O(g)△H=-1076.7kJ/mol |
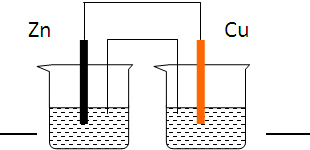 总反应:Zn+Cu2+=Zn2++Cu.
总反应:Zn+Cu2+=Zn2++Cu.