题目内容
【题目】在两个容积相同的容器中,一个盛有HCl气体,另一个盛有H2和Cl2的混合气体.在同温、同压下,两容器内的气体一定具有相同的是( )
A.原子数
B.相对分子质量
C.质量
D.密度
【答案】A
【解析】解:同温同压下,气体摩尔体积相等,体积相等的不同气体其物质的量相等.A.根据N=nNA知,二者的物质的量与分子数成正比,物质的量相等则其分子数相等,每个分子中原子个数相等,所以其原子总数相等,故A正确;
B.盛有H2和Cl2的混合气体的容器中两种气体的物质的量的关系不知道,所以不能求出混合气体的平均摩尔质量,则二者的摩尔质量不一定相等,故B错误;
C.根据m=nM知,物质的量相等时,二者的质量与其摩尔质量成正比,二者的摩尔质量不一定相等,所以其质量不一定相等,故C错误;
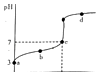
D.根据ρ= ![]() 知,密度与其摩尔质量成正比,两个容器中平均摩尔质量不一定相等,所以其密度不一定相等,故D错误;
知,密度与其摩尔质量成正比,两个容器中平均摩尔质量不一定相等,所以其密度不一定相等,故D错误;
故选:A.

【题目】在证明海带中存在碘元素的实验操作中,主要仪器选用错误的是( )
选项 | 操作 | 主要仪器 |
A | 称取3.0g干海带 | 托盘天平 |
B | 灼烧干海带至完全变成灰烬 | 蒸发皿 |
C | 过滤煮沸后的海带灰与水的混合液 | 漏斗 |
D | 用四氯化碳从氧化后的海带灰浸取液中提取碘 | 分液漏斗 |
A.AB.BC.CD.D
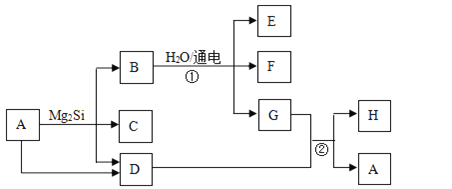
【题目】为增强铝的耐腐蚀性,现以铅蓄电池为外电源,以Al作阳极、Pb作阴极,电解稀硫酸,使铝表面的氧化膜增厚.其反应原理如下:电池:Pb(s)+PbO2(s)+2H2SO4(aq)=2PbSO4(s)+2H2O(l);电解池:2Al+3H2O ![]() Al2O3+3H2↑,电解过程中,以下判断正确的是( )
Al2O3+3H2↑,电解过程中,以下判断正确的是( )
电池 | 电解池 | |
A | H+移向Pb电极 | H+移向Pb电极 |
B | 每消耗3molPb | 生成2molAl2O3 |
C | 正极:PbO2+4H++2e﹣=Pb2++2H2O | 阳极:2Al+3H2O﹣6e﹣=Al2O3+6H+ |
D |
|
|
A.A
B.B
C.C
D.D