题目内容
8. 某物质的晶体中含A、B、C三种元素,其排列方式如图所示(其中前后两面心上的B原子未画出),晶体中A、B、C的原子个数之比依次为( )
某物质的晶体中含A、B、C三种元素,其排列方式如图所示(其中前后两面心上的B原子未画出),晶体中A、B、C的原子个数之比依次为( )| A. | 1:3:1 | B. | 2:3:1 | C. | 2:2:1 | D. | 1:3:3 |
分析 该晶胞中位于体心上的原子被一个晶胞占有、位于顶点上的原子被8个晶胞占有、位于棱上的原子被4个晶胞占有,利用均摊法计算各种原子个数.
解答 解:该晶胞中位于体心上的原子被一个晶胞占有、位于顶点上的原子被8个晶胞占有、位于棱上的原子被4个晶胞占有,所以该晶胞中A原子个数=8×$\frac{1}{8}$=1、B原子个数=12×$\frac{1}{4}$=3、C原子个数=1,所以晶体中A、B、C的原子个数之比=1:3:1,故选A.
点评 本题考查晶胞计算,侧重考查学生空间想象能力及计算能力,明确每个原子被几个晶胞占有是解本题关键,题目难度不大.

练习册系列答案
 芝麻开花课程新体验系列答案
芝麻开花课程新体验系列答案 怎样学好牛津英语系列答案
怎样学好牛津英语系列答案
相关题目
18.下列化学用语中正确的是( )
| A. | ${\;}_{8}^{18}$O2-离子结构示意图: | B. | NH4Cl的电子式: | ||
| C. | 含78个中子的碘的核素:53131I | D. | 二氧化硅的分子式:SiO2 |
19.下列各组气体通常条件下能稳定共存( )
| A. | NH3 O2 HCl | B. | H2S O2 SO2 | C. | CO2 HI Cl2 | D. | N2 H2 HCl |
16.已知反应A(g)+3B(g)═2C(g)+D(g)在某段时间内以A的浓度变化表示的化学反应速率为1mol/(L•min),则此段时间内以C的浓度变化表示的化学反应速率为( )
| A. | 0.5 mol/(L•min) | B. | 1 mol/(L•min) | C. | 2 mol/(L•min) | D. | 3 mol/(L•min) |
13.在密闭容器中进行如下可逆反应:X2(g)+Y2(g)?2XY(g),已知X2、Y2、XY三者起始浓度分别为0.1mol/L、0.3mol/L、0.2mol/L,在一定条件下反应处于平衡,此时容器中不可能的情况是( )
| A. | XY为0.3mol/L | B. | Y2为0.35mol/L | ||
| C. | X2为0.2mol/L | D. | X2、Y2、XY总浓度为0.6mol/L |
17.短周期元素R、W、X、Y、Z的原子序数依次增大,R原子的最外层电子数是其内层电子数的2倍,X元素的焰色反应呈黄色,W元素和Z元素同主族,且Z元素的核电荷数是W的2倍,Y是地壳中除氧外含量最多的非金属元素.下列说法不正确的是( )
| A. | W与X形成的两种化合物中阴、阳离子的个数比均为1:2 | |
| B. | Y、R、Z最高价氧化物对应水化物的酸性强弱顺序:Z>R>Y | |
| C. | W的氢化物熔沸点比Z的氢化物熔沸点低 | |
| D. | Y与R形成的化合物YR的熔点高、硬度大 |
18.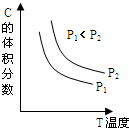 已知某可逆反应aA(g)+bB(g)?cC(g)+dD(l);△H=-E KJ•mol-1.反应过程中,当其它条件不变时,C的体积分数与温度(T)和压强(P)的关系如图.下列叙述正确的是( )
已知某可逆反应aA(g)+bB(g)?cC(g)+dD(l);△H=-E KJ•mol-1.反应过程中,当其它条件不变时,C的体积分数与温度(T)和压强(P)的关系如图.下列叙述正确的是( )
 已知某可逆反应aA(g)+bB(g)?cC(g)+dD(l);△H=-E KJ•mol-1.反应过程中,当其它条件不变时,C的体积分数与温度(T)和压强(P)的关系如图.下列叙述正确的是( )
已知某可逆反应aA(g)+bB(g)?cC(g)+dD(l);△H=-E KJ•mol-1.反应过程中,当其它条件不变时,C的体积分数与温度(T)和压强(P)的关系如图.下列叙述正确的是( )| A. | 正反应为吸热反应 | |
| B. | 100摄氏度时,当生成cmolC,放出E KJ热量 | |
| C. | a+b<c+d | |
| D. | 降低压强,正、逆反应速率都减小 |
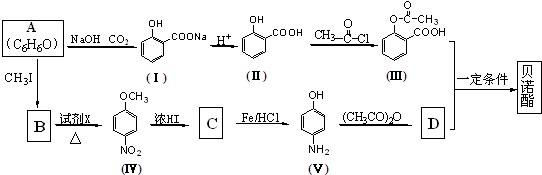
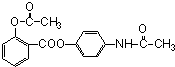
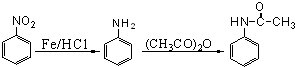
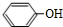 ;
; 或
或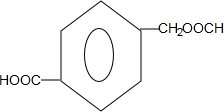 ;
;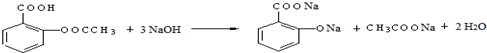 ;
;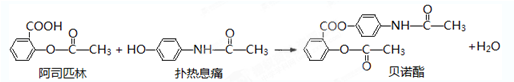 .
.