题目内容
【题目】碳及其化合物广泛存在于自然界。请回答下列问题:
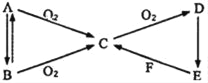
(1)反应Ⅰ:Fe(s)+CO2(g)![]() FeO(s)+CO(g) ΔH1 平衡常数为K1
FeO(s)+CO(g) ΔH1 平衡常数为K1
反应Ⅱ:Fe(s)+H2O(g)![]() FeO(s)+H2(g) ΔH1 平衡常数为K2
FeO(s)+H2(g) ΔH1 平衡常数为K2
不同温度下,K1、K2的值如下表:
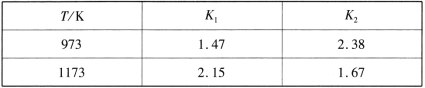
现有反应Ⅲ:H2(g)+CO2(g)![]() CO(g)+H2O(g),结合上表数据,反应Ⅲ是___(填“放热”或“吸热”)反应,为提高CO2的转化率可采用措施有___(写出任意两条)。
CO(g)+H2O(g),结合上表数据,反应Ⅲ是___(填“放热”或“吸热”)反应,为提高CO2的转化率可采用措施有___(写出任意两条)。
(2)已知CO2催化加氢合成乙醇的反应原理为:2CO2(g)+6H2(g)![]() C2H5OH(g)+3H2O(g) H<0。设m为起始时的投料比,即m= n(H2)/ n(CO2)。
C2H5OH(g)+3H2O(g) H<0。设m为起始时的投料比,即m= n(H2)/ n(CO2)。
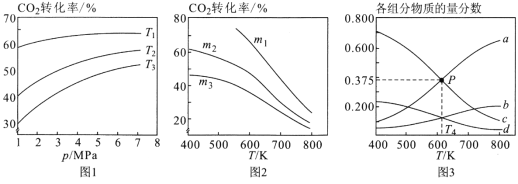
①图1中投料比相同,温度从高到低的顺序为______。
②图2中m1、m2、m3从大到小的顺序为____。
③图3表示在总压为5MPa的恒压条件下,且m=3时,平衡状态时各物质的物质的量分数与温度的关系。则曲线d代表的物质化学名称为____,T4温度时,该反应平衡常数KP的计算式为____。
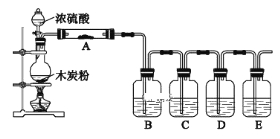
(3)工业上常用高浓度的 K2CO3溶液吸收CO2,得溶液X,再利用电解法使K2CO3溶液再生,其装置示意图如图:
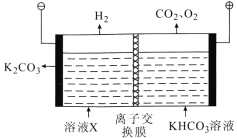
①在阳极区发生的反应包括____和H++HCO3- ==CO2↑+H2O
②简述CO32-在阴极区再生的原理:____。
【答案】吸热 升高温度、提高氢气浓度、吸收CO、液化水蒸气(任选两条) ![]()
![]() 乙醇
乙醇 ![]()
![]() 阴极水电解生成氢气和氢氧根离子,
阴极水电解生成氢气和氢氧根离子,![]() 与
与![]() 反应生成
反应生成![]()
【解析】
(1)![]() ,则
,则![]() ,所以973K时,
,所以973K时,![]() ,1173K时,
,1173K时,![]() ,升高温度,平衡常数增大,所以正反应为吸热反应,提高CO2的转化率可采用措施有高温度、提高氢气浓度、吸收CO、液化水蒸气,任选两条答题即可;
,升高温度,平衡常数增大,所以正反应为吸热反应,提高CO2的转化率可采用措施有高温度、提高氢气浓度、吸收CO、液化水蒸气,任选两条答题即可;
(2)①正反应放热,温度越高,二氧化碳的平衡转化率越小,所以温度从高到低的顺序为![]() ;
;
②增大n(H2),平衡正向移动,二氧化碳的平衡转化率越大,所以![]() ;
;
③升高温度,平衡逆向移动,二氧化碳和氢气的含量增大,乙醇、水减少,乙醇的含量是水的![]() ,所以曲线d代表的物质为乙醇,化学反应的压强平衡常数为生成物分压的幂之积除以反应物分压的幂之积,体系中各组分的分压=该物质的物质的量分数×体系总压强,故该反应平衡常数KP的计算式为
,所以曲线d代表的物质为乙醇,化学反应的压强平衡常数为生成物分压的幂之积除以反应物分压的幂之积,体系中各组分的分压=该物质的物质的量分数×体系总压强,故该反应平衡常数KP的计算式为![]() ;
;
(3)①装置图分析与电源正极相连的为电解池的阳极,与电源负极相连的为电解池的阴极,阳极上是氢氧根离子失电子生成氧气,电极反应为:4OH--4e-═2H2O+O2↑(或2H2O-4e-=4H++O2↑),生成的氢离子与HCO3-反应生成二氧化碳气体;
②在阴极区,溶液中H+放电,破坏水的电离平衡,OH-浓度增大,OH-与HCO3-反应生成CO32-,所以CO32-再生。

 名校课堂系列答案
名校课堂系列答案【题目】标号为①~⑩的元素,在元素周期表中的位置如下:
主族 周期 | ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | 0族 |
1 | ① | ② | ||||||
2 | ③ | ④ | ⑤ | ⑥ | ||||
3 | ⑦ | ⑧ | ⑨ | ⑩ |
试回答下列问题:
(1)(填写元素符号)① _____③______⑤_____ ⑦_____
(2)①和④号元素形成的化合物的化学式________,用电子式表示其形成过程为__________。
(3)⑦和⑧号元素的最高价氧化物的水化物的碱性是: ______﹥_________ (填化学式)。⑨和⑩号元素的最高价氧化物的水化物的酸性是: ______ ﹥_________ (填化学式)。
(4)①、⑤、⑦号元素形成的一种化合物的电子式是________,在该化合物中既含有________键,又含有________键。