题目内容
【题目】下列图示与对应的叙述相符的是( )
A.图甲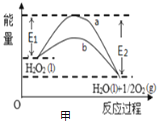 中,b曲线的热化学方程式为:H2O2(l)=H2O(l)+
中,b曲线的热化学方程式为:H2O2(l)=H2O(l)+![]() O2(g)△H=(E1-E2)kJ/mol
O2(g)△H=(E1-E2)kJ/mol
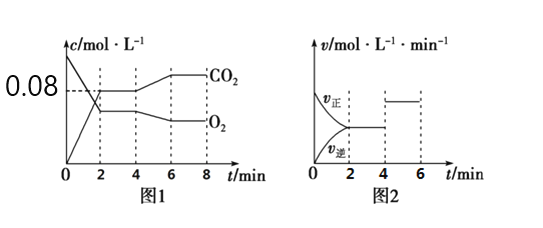
B.图乙 表示氢氟酸为弱酸,且a点
表示氢氟酸为弱酸,且a点![]() 的数值比b点
的数值比b点![]() 数值大
数值大
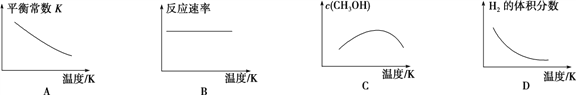
C.图丙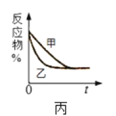 表示压强对可逆反应2A(g)+2B(g)
表示压强对可逆反应2A(g)+2B(g)![]() 3C(g)+D(s)的影响,乙的压强比甲的压强大
3C(g)+D(s)的影响,乙的压强比甲的压强大
D.图丁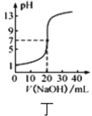 表示
表示![]() 溶液滴定
溶液滴定![]() 醋酸溶液的滴定曲线
醋酸溶液的滴定曲线
【答案】A
【解析】
A.图示中的各物质计量数与热化学方程式相同,焓变等于正反应的活化能与逆反应的活化能之差,A项正确;
B.盐酸是强酸,对比可知氢氟酸是弱酸;a、b两点对应的温度相同,所以Kw应相同,B项错误;
C.横轴表示时间,“先拐先平数值大”,即乙的压强比甲的压强大,该反应是正向气体分子数减小的反应(注意D为固体),乙相对于甲来说相当于加压,加压,该平衡正向移动,反应物的含量降低,而所给图示中甲、乙条件下反应物的含量是相等的,C项错误;
D.因醋酸是弱酸,所以当加入20mLNaOH溶液时,刚好反应完全,生成醋酸钠溶液,此时溶液显碱性而不是pH=7,D项错误;
所以答案选择A项。

【题目】在通风橱中进行下列实验:
实验 步骤 |
|
|
|
|
现象 | Fe表面产生大量 无色气体,在液面 上方变红棕色 | Fe表面无明 显变化 | 常温下有无色气泡,加热后,Cu表面产生无色气体,在液面上方变红棕色 | Cu表面产生红 棕色气体 |
请回答下列问题:
(1)①中气体由无色变为红棕色,红棕色气体是__________________(填分子式)。
(2)②中的现象说明Fe发生了______现象,产生的原因是________________________。
(3)对比①②中的现象,______(填“能”或“不能”)说明稀硝酸的氧化性强于浓硝酸。
(4)对比③④中的现象,说明氧化性:稀硝酸______(填“>”或“<”)浓硝酸。
(5)③中在加热时的化学反应方程式为________________________,此反应中稀硝酸除表现出氧化性外,还表现出____________。
【题目】金属钛(Ti)因其硬度大、熔点高、常温时耐酸碱腐蚀而被广泛用作高新科技材料,被誉为“未来金属”。以钛铁矿(主要成分钛酸亚铁)为主要原料冶炼金属钛同时获得副产品甲的工业生产流程如下。请回答下列问题。

(1)钛酸亚铁(用R表示)与碳在高温下反应的化学方程式为2R+C═2Fe+2TiO2+CO2↑,钛酸亚铁的化学式为_______________;钛酸亚铁和浓H2SO4反应的产物之一是TiOSO4,反应中无气体生成,该反应的化学方程式为_____________________________________。
(2)上述生产流程中溶液Ⅰ中含有Fe2+、TiO2+和少量Mg2+等阳离子。常温下,其对应氢氧化物的Ksp如下表所示。
氢氧化物 | Fe(OH)2 | TiO(OH)2 | Mg(OH)2 |
Ksp | 8.0×10-16 | 1.0×10-29 | 1.8×10-11 |
①常温下,若所得溶液中Mg2+的物质的量浓度为0.0018mol/L,当溶液的pH等于_______时,Mg(OH)2开始沉淀。
②若将含有Fe2+、TiO2+和Mg2+的溶液加水稀释,立即析出大量白色沉淀,该反应的离子方程式为___________________________________________________________。
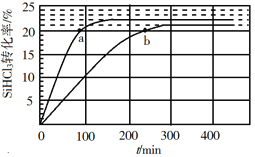
(3)中间产品乙与焦炭、氯气在高温下发生反应制取TiCl4的方程式为______________。Mg还原TiCl4过程中必须在1070K的温度下进行,你认为还应该控制的反应条件是_________。
【题目】现有七种元素A、B、C、D、E、F、G,其中A、B、C为三个不同周期的短周期元素,E、F、G为第四周期元素。请根据下列相关信息,回答问题。
A元素的核外电子数和电子层数相等,也是宇宙中最丰富的元素 |
B元素原子的核外p电子数与s电子数相等 |
C基态原子的价电子排布为nsn-1npn+1 |
D的能层数与C相同,且电负性比C大 |
E元素的主族序数与周期数的差为1,且第一电离能比同周期相邻两种元素都大 |
F是前四周期中电负性最小的元素 |
G在周期表的第五列 |
(1)C基态原子中能量最高的电子,其电子云在空间有____个方向,原子轨道呈____形,C简单离子核外有___种运动状态不同的电子。
(2)①一般情况下,同种物质为固态时密度大于其液态,但固态A2B的密度比其液态时小,原因是___;
②A2B2难溶于CS2,简要说明理由:________。
(3)G位于____族___区,它的一种氧化物常用于工业生产硫酸的催化剂,已知G在该氧化物中的化合价等于其价电子数,则该氧化物的化学式为____;
(4)ED3分子的VSEPR模型名称为____,其中E原子的杂化轨道类型为____。
【题目】根据下列实验操作和现象所得出的结论正确的是
选项 | 实验操作和现象 | 结论 |
A | 向苯酚浊液中滴加Na2CO3溶液,浊液变清 | 苯酚的酸性强于H2CO3的酸性 |
B | 向碘水中加入等体积CCl4,振荡后静置,上层接近无色,下层显紫红色 | I2在CCl4中的溶解度大于在水中的溶解度 |
C | 向CuSO4溶液中加入铁粉,有红色固体析出 | Fe2+的氧化性强于Cu2+的氧化性 |
D | 向NaCl、NaI的混合稀溶液中滴入少量稀AgNO3溶液,有黄色沉淀生成 | Ksp(AgCl) >Ksp(AgI) |
A. A B. B C. C D. D