题目内容
15.下列热化学方程式中△H代表燃烧热的是( )| A. | C6H12O6(s)+6O2(g)=6CO2(g)+6H2O(l)△H1 | B. | S(s)+3/2O2(g)=SO3(s)△H2 | ||
| C. | CH4(g)+2O2(g)=2H2O(l)+CO(g)△H3 | D. | 2CO(g)+O2(g)=CO2(g)△H4 |
分析 燃烧热是指1mol可燃物完全燃烧生成稳定的氧化物放出的热量,据此解答.
解答 解:A.符合燃烧热的定义,热化学方程式中△H代表燃烧热,故A正确;
B.硫与氧气反应生成产物为二氧化硫,得不到三氧化硫,故B错误;
C.甲烷燃烧生成的二氧化碳和液态水是稳定的氧化物,热化学方程式中生成的是一氧化碳,所以△H代表燃烧热,故C错误;
D.热化学方程式中CO的物质的量不为1mol,热化学方程式中△H不等于燃烧热,故D错误;
故选:A.
点评 本题考查了燃烧热的判断,熟悉燃烧热的概念是解题关键,题目难度不大.

练习册系列答案
相关题目
6.实验室用铅蓄电池作电源电解饱和食盐水制取氯气,已知铅蓄电池放电时发生如下反应:
负极:Pb+SO42-=PbSO4+2e-
正极:PbO2+4H++SO42-+2e-=PbSO4+2H2O
今若制得Cl2 0.10mol,这时电池内消耗的H2SO4的物质的量至少是( )
负极:Pb+SO42-=PbSO4+2e-
正极:PbO2+4H++SO42-+2e-=PbSO4+2H2O
今若制得Cl2 0.10mol,这时电池内消耗的H2SO4的物质的量至少是( )
| A. | 0.025 mol | B. | 0.050 mol | C. | 0.10 mol | D. | 0.20 mol |
3.下列关于烃的性质说法中正确的是( )
| A. | 苯和甲苯都能与浓硝酸发生苯环上的取代反应 | |
| B. | 苯和甲苯都能使酸性高锰酸钾溶液褪色 | |
| C. | 苯和己炔都能使溴的四氯化碳溶液发生化学反应而褪色 | |
| D. | 苯和乙烷与卤素单质发生取代反应都需要铁作催化剂 |
20.下列说法正确的是( )
| A. | H、N、Na、Fe、V五种元素中,有两种是第四周期元素 | |
| B. | 铁元素位于周期表中的第四周期,第8纵行,属于第ⅧA族 | |
| C. | 第四、五、六、七周期,每周期的元素共有18种 | |
| D. | 碱金属元素是指第ⅠA族的所有元素 |
7.下列对化学知识概括合理的是( )
| A. | 金属氧化物都是强电解质 | |
| B. | 一种金属元素只能有一种氧化物 | |
| C. | 在化学反应中,一定有化学键的断裂和形成,并伴有能量的变化 | |
| D. | 能与金属铝反应产生氢气的溶液一定是酸溶液 |
4.下列物质中含离子键的是( )
| A. | 石英 | B. | 食盐 | C. | 干冰 | D. | 碘 |
5.已知A、B、C、D四种短周期主族元素,其相关信息如下:
①在元素周期表中的相对位置如下:
②B元素原子的最外层电子数为其核外电子总数的$\frac{2}{7}$,D的单质在空气中燃烧时,生成对环境有严重污染的气体.
请回答下列问题:
(1)D的元素符号为S,B的原子结构示意图为 .
.
(2)C的最高价氧化物对应水化物的化学式为H3PO4.
(3)下列说法中正确的是abc(填字母).
a.A的最高价氧化物对应的水化物在常温下可以和铜反应
b.B的最高价氧化物对应水化物钠盐的水溶液俗称水玻璃
c.常温下,D的最高价氧化物对应水化物的浓溶液可用铁制容器盛放
d.C的离子半径小于D的离子半径
(4)探究法是学习化学的重要方法之一.在下表中列出了对H2DO3各种不同化学性质的推测,根据示例完成下列表格:
①在元素周期表中的相对位置如下:
| A | ||
| B | C | D |
请回答下列问题:
(1)D的元素符号为S,B的原子结构示意图为
 .
.(2)C的最高价氧化物对应水化物的化学式为H3PO4.
(3)下列说法中正确的是abc(填字母).
a.A的最高价氧化物对应的水化物在常温下可以和铜反应
b.B的最高价氧化物对应水化物钠盐的水溶液俗称水玻璃
c.常温下,D的最高价氧化物对应水化物的浓溶液可用铁制容器盛放
d.C的离子半径小于D的离子半径
(4)探究法是学习化学的重要方法之一.在下表中列出了对H2DO3各种不同化学性质的推测,根据示例完成下列表格:
| 编号 | 性质推测 | 化学方程式 |
| 示例 | 氧化性 | H2DO3+2H2D=3D↓+3H2O |
| ① | 酸性 | |
| ② | H2DO3+Br2+H2O=H2DO4+2HBr |
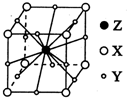 X、Y、Z、W为短周期元素且原子序数依次增大.X的一种气态氢化物m可用来焊接或切割金属,且该分子所有原子在一条直线上.Y2-的M能层的原子轨道为全空状态.Z的单质用作铝热反应的引燃剂. W与X形成的化合物是一种常见的有机溶剂n.A为第四周期元素,其基态原子含有6个未成对电子.
X、Y、Z、W为短周期元素且原子序数依次增大.X的一种气态氢化物m可用来焊接或切割金属,且该分子所有原子在一条直线上.Y2-的M能层的原子轨道为全空状态.Z的单质用作铝热反应的引燃剂. W与X形成的化合物是一种常见的有机溶剂n.A为第四周期元素,其基态原子含有6个未成对电子.