题目内容
4.现有标准状况下的氮气5.6克,下列说法正确的是( )| A. | 它的体积为2.24L | B. | 其摩尔体积为22.4L.mol-1 | ||
| C. | 含有氮分子数为0.4NA | D. | 其摩尔质量为28mol |
分析 根据n=$\frac{m}{M}$=$\frac{N}{{N}_{A}}$=$\frac{V}{{V}_{m}}$计算.
解答 解:n=$\frac{5.6g}{28g/mol}$=0.2mol,
A.V=0.2mol×22.4L/mol=4.48L,故A错误;
B.标准状况下,摩尔体积为22.4L.mol-1,故B正确;
C.N=0.2mol×NA/mol=0.2NA,故C错误;
D.摩尔质量为28g/mol,故D错误.
故选B.
点评 本题综合考查物质的量的计算,为高频考点,侧重于学生的分析、计算能力的考查,注意把握相关计算公式的运用,难度不大.

练习册系列答案
 黄冈冠军课课练系列答案
黄冈冠军课课练系列答案
相关题目
15.将一定量的金属钠放入一定浓度的氢氧化钠溶液中,反应完全后,恢复到原温度,氢氧化钠的浓度( )
| A. | 增大 | B. | 减小 | C. | 不变 | D. | 不能确定 |
19.设NA为阿伏伽德罗常数,下列说法不正确的是( )
| A. | 含1 mol FeCl3的饱和溶液最多可形成胶体粒子数为NA | |
| B. | 4.6 g Na与稀盐酸反应,转移电子数一定为0.2NA | |
| C. | 10.6 g Na2C03晶体中含CO${\;}_{3}^{2-}$数目为0.1NA | |
| D. | 常温下,22g CO2含碳氧双键数目为NA |
16.下列说法不正确的是( )
| A. | 蛋白质溶液中加入饱和硫酸铵溶液后产生的沉淀能重新溶于水 | |
| B. | CH2=CH-CH(CH3)-C≡CH经催化加氢可生成3-甲基戊烷 | |
| C. | 当人误食重金属盐类时,可以喝大量的牛奶、蛋清解毒 | |
| D. | 已知苹果酸的结构简式为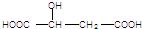 ,则该物质可发生氧化反应、酯化反应、缩聚反应,与HOOC-CH2-CH(OH)-COOH互为同分异构体 ,则该物质可发生氧化反应、酯化反应、缩聚反应,与HOOC-CH2-CH(OH)-COOH互为同分异构体 |
13.设NA表示阿伏伽德罗常数,下列说法中正确的 ( )
| A. | 1mol OH-含有电子数目为9NA | |
| B. | 71g 37Cl2所含中子数目为40NA | |
| C. | 1mol铁和1mol Cl2完全反应,转移的电子数目为3NA | |
| D. | 1mol Cl2和氢氧化钠完反应,转移的电子数目为NA |