题目内容
【题目】为将反应2Al+6H+═2Al3++3H2↑的化学能转化为电能,下列装置能达到目的是(铝条均已除去了氧化膜)
A. 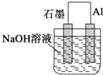 B.
B. 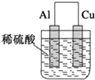 C.
C. 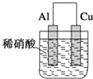 D.
D. 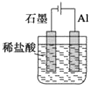
【答案】B
【解析】分析:将反应2Al+6H+=2Al3++3H2↑的化学能转化为电能,需要形成原电池,并且铝为负极,电解质溶液为非氧化性稀酸,据此判断。
详解:A.为原电池,铝为负极,但总反应为:2Al+2OH-+2H2O=2AlO2-+3H2↑,A不符合;
B.为原电池,铝的金属性强于铜,铝为负极,总反应为2Al+6H+=2Al3++3H2↑,B符合;
C.为原电池,但硝酸是氧化性酸,则总反应为Al+4H++NO3-=Al3++NO↑+2H2O,C不符合;
D.装置中有外接电源,为电解池,D不符合;答案选B。

练习册系列答案
 期末冲刺100分创新金卷完全试卷系列答案
期末冲刺100分创新金卷完全试卷系列答案
相关题目
【题目】试回答下列各题:
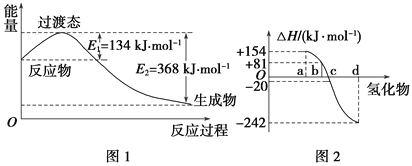
(1)如图1所示是NO2和CO反应生成CO2和NO过程中能量变化示意图,请写出NO2和CO反应的热化学方程式: ______________________________。
(2)化学反应的焓变与反应物和生成物的键能有关。
①已知:H2(g)+Cl2(g)===2HCl(g) ΔH=-185 kJ·mol-1
请填空:
共价键 | H—H | Cl—Cl | H—Cl |
键能/(kJ·mol-1) | 436 | 247 | ________ |
②图2中表示氧族元素中氧、硫、硒、碲生成氢化物时的焓变数据,根据焓变数据可确定a、b、c、d分别代表哪种元素,试写出硒化氢在热力学标准状态下,发生分解反应的热化学方程式: ___________________________________。