题目内容
【题目】下列有关NaHCO3溶液的说法正确的是
A. 该溶液中,H+、Al3+、Cl-能大量共存 B. 该溶液中c(H2CO3)<c(CO32-)
C. 该溶液中阳离子总数大于阴离子总数 D. 常温下,加水稀释,  变小
变小
【答案】C
【解析】A. HCO3-与H+反应生成二氧化碳和水而不能大量共存,HCO3-与Al3+发生双水解生成沉淀和气体而不能大量共存,选项A错误;B. NaHCO3溶液中HCO3-的水解大于电离,故c(H2CO3)>c(CO32-),选项B错误;C. 根据电荷守恒有c(Na+)+c(H+)=2(CO32-)+c(HCO3-)+c(OH-),故c(Na+)+c(H+)>(CO32-)+c(HCO3-)+c(OH-),即该溶液中阳离子总数大于阴离子总数,选项C正确;D. 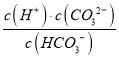 为HCO3-的电离平衡常数的表达式,温度不变,电离平衡常数不变,常温下,加水稀释,
为HCO3-的电离平衡常数的表达式,温度不变,电离平衡常数不变,常温下,加水稀释, 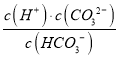 不变,选项D错误。答案选C。
不变,选项D错误。答案选C。

练习册系列答案
相关题目