��Ŀ����
����Ŀ��ͭ���ҹ���ɫ�������ϵ������н�������,�㷺��Ӧ���ڵ�������е���졢���������ش���������:
��1���þ����X�������䷨���Բ�ð����ӵ��������Խ���ͭ�IJⶨ�õ����½��:����Ϊ�����������ܶѻ�,�߳�Ϊ361 pm����֪ͭ���ܶ�Ϊ9.00 g��cm-3,�����ӵ�����Ϊ__________ (��ʽ����,��֪Ar(Cu)=63.6);
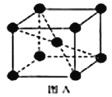
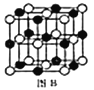
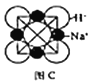
��2���Ⱥͼ��벻ͬ��̬��ͭ���������ֻ�����,�����ֻ����ﶼ�����ڴ���Ȳ�ۺ�,�������Ӿ�Ϊ�������ṹ(����ͼ),aλ����Clԭ�ӵ��ӻ��������Ϊ______����֪����һ�ֻ�����Ļ�ѧʽΪKCuCl3,��һ�ֵĻ�ѧʽΪ_______;

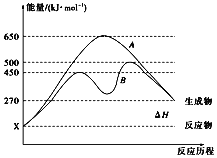
��3������ͭ�����백ˮ����������ⶼ���ܷ�Ӧ,�����백ˮ��������Ļ����Һ��Ӧ,��ԭ����___________,��Ӧ�Ļ�ѧ����ʽΪ______________��
���𰸡� NA=6.01��1023 mol-1 sp3 K2CuCl3 ��������Ϊ������,����Cu2+�γ�������,������ٽ�ʹ��Ӧ���� Cu+H2O2+4NH3Cu(NH3��22++2OH-
����������1�����������������ı߳�Ϊa���������Ϊa3��ÿ�����������ĸ�ԭ���������ĸ�ԭ�ӵ�����Ϊ4M/NA��MΪ��ԭ�ӵ����ԭ�������������Ծ����ܶ�Ϊ��=4M/ a3NA������=9.00 g��cm-3��a=361pm��M=63.6,������ʽ���Լ���NA=6.01��1023 mol-1��
��2��aλ����Clԭ�ӳ�2������������2�Թ¶Ե��ӣ��ӻ������Ϊ4���ӻ��������Ϊsp3��һ�ֻ�����Ļ�ѧʽΪKCuCl3������ͭԪ��Ϊ+2�ۣ�����һ�ֻ�������ͭΪ+1�ۣ������ӹ�����[CuCl3]��һ��������ΪCuΪ+1��������Ӧ��Ϊ[CuCl3]2�����仯ѧʽΪ��K2CuCl3��
��3����ˮ������������ͭ��������Ӧ����ͬʱ����ܷ�Ӧ��˵�������ܻ���ٽ���Ӧ�����������ʹ�ͬ���õĽ����������������Ϊ������������Cu2+�γ������ӣ�������ٽ�ʹ��Ӧ���У�����ʽ�ɱ�ʾΪ��Cu+H2O2 +4NH3�TCu(NH3)42++2OH����

 ��ĩ�óɼ�ϵ�д�
��ĩ�óɼ�ϵ�д� 99��1������ĩ��ѵ��ϵ�д�
99��1������ĩ��ѵ��ϵ�д� ��ǿ��У��ĩ���100��ϵ�д�
��ǿ��У��ĩ���100��ϵ�д� �óɼ�1��1��ĩ���100��ϵ�д�
�óɼ�1��1��ĩ���100��ϵ�д� ��״Ԫ���źþ�ϵ�д�
��״Ԫ���źþ�ϵ�д�����Ŀ����Ʒ�����ʵ��̽���ı�֤��������̽���ĸ���Ŀ�ġ�ij����ѧϰС�鿪չ������̽����
ʵ��һ����������������Һ���Ƿ����������ơ�
��������������Ͽ����������ƺ��������ƶ����ڼ������ˮ��Һ�ж��ܽ������ͬ��_______������ţ������Ծ������ƵĻ�ѧ���ʡ������ڽ������Na+��Ca2+��ͬ����������Ҳ�в�ͬ�����ʵ��ʱ�ɼ����ܽ����CO32�����Լ�����CO32����Ca2+��ϲ�����ɫ������һ�����������Լ��顣
����Ʒ�����ʵ�飩
ʵ����� | ���� | ���� | |
����һ | ȡ����������Һ���Թ��У�ͨ��CO2 | ���ְ�ɫ���� | ����������Һ�к����������� |
������ | ȡ����������Һ���Թ��У��μ� _________��Һ | ���ְ�ɫ���� |
д�����������г��ְ�ɫ������һ����ѧ����ʽ__________________________________________��
�����������ڼ�������ʱ��Ҫ�������ʵ���ɺ�______���ݴ�ѡ�����ǡ�����Լ��������ݲ�ͬ����ó����ۡ�
��ʵ��̽����ʵ�������һ����ɫ���壬���ܺ����Ȼ��ơ��������ơ�̼���ơ������ƺ����ᱵ�е�һ�ֻ��֣�Ϊ̽������ɣ�ij����ѧϰС����Ʒ���������������ʵ�飺
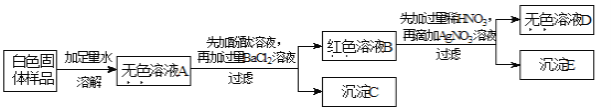
��1������ʵ���У����˲����õ��IJ��������У��ձ�����������_________��
��2��С��ͬѧͨ������ʵ����֪����ɫ������Ʒ��һ��������_________�����ѧʽ��
��3��Ϊȷ����ɫ������Ʒ�п��ܴ��ڵ����ʣ�С��Գ���C����ʵ�顣
ʵ����� | ���� | ���� |
ȡ��������C���Թ��У�������� _________�� | �����ݲ���������ȫ����ʧ�� | ��ɫ������Ʒ��һ������ ________�� |
��4��С��ͬѧ��Ϊ��ɫ�����л�Ҫ���ʲ���ȷ�����Ƿ���ڣ��������ǣ�_________________��
���û�ѧ����ʽ��ʾ����Ҫȷ�ϣ�ֻ�轫����ʵ�鷽�������ӵ�һ���Լ���Ϊ_______���ɡ�
�������������������ʵĴ��ڶ�������������и���ʱ�����Ƚ���������ת������ѡ�����ǡ�����Լ��������ݲ�ͬ����ó����ۡ�
����Ŀ����һ���¶��£�������X������Y��0.32mol����10L�����ܱ������У�������Ӧx(g)+ Y(g) ![]() 2Z(g)AH<0��һ��ʱ���ﵽƽ�⡣��Ӧ�����вⶨ���������±���
2Z(g)AH<0��һ��ʱ���ﵽƽ�⡣��Ӧ�����вⶨ���������±���
t/min | 2 | 4 | 7 | 9 |
n(Y)/mol | 0.24 | 0.22 | 0.20 | 0.20 |
����˵����ȷ������ ��
A. ��Ӧǰ2min ��ƽ������ v(Z)=4.0��10-3mol/(L��min)
B. �����������䣬�����¶ȣ���Ӧ�ﵽ��ƽ��ǰv������>v������
C. ���¶��´˷�Ӧ��ƽ�ⳣ��k=1.44
D. �����������䣬�ٳ���0.2molZ��ƽ��ʱX�����������С