题目内容
4.实验室部分仪器或装置如图1所示,请回答下列问题.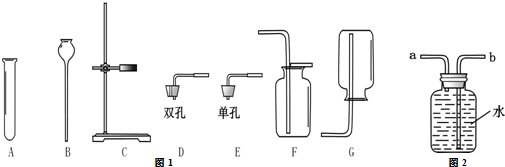
(1)若要组装一套二氧化碳气体的发生和收集的装置,可选择图2中的ACEF(填标号).实验
室制取二氧化碳的化学方程式为CaCO3+2HCl═CaCl2+H2O+CO2↑.
(2)用该装置还可以制取的气体是氧气,选择气体的发生装置应考虑的因素是反应物状态和反应条件.
(3)若用高锰酸钾制取氧气,你认为还需要增加的仪器是酒精灯,
用图2所示装置收集氧气,氧气应从a(填“a”或“b”)端导入.
分析 依据反应物的状态与反应的条件选择发生装置,实验室制取氧气、氢气、二氧化碳都可用固液常温型装置制取,用高锰酸钾加热制取氧气,需要加热,排水法收集气体应短进长出,据此解答.
解答 解:(1)实验室用固体碳酸钙与盐酸反应制取二氧化碳,方程式:CaCO3+2HCl═CaCl2+H2O+CO2↑,反应不需要加热,实验室制取二氧化碳属于固液常温型,所以选择试管、铁架台、单孔塞,氧气、二氧化碳的密度比空气大,所以都可用向上排空气法收集;
故答案为:ACEF;
(2)该装置制备气体特点:固体+液体不加热,用该装置还可以制取的气体是氧气,发生装置的选择应考虑:反应物的状态和反应的条件;
故答案为:氧气;反应物的状态和反应的条件;
(3)实验室用高锰酸钾或氯酸钾制氧气都需加热,所以需酒精灯;排水法收集气体应短进长出,
故答案为:酒精灯;a.
点评 本题考查了化学实验基本原理(气体的制备)、实验装置、仪器的使用,题目难度中等,熟悉制备原理和装置选择的依据是解题关键.

练习册系列答案
 夺冠金卷全能练考系列答案
夺冠金卷全能练考系列答案
相关题目
14. 已知气体的摩尔质量越小,扩散速度越快.如图所示为气体扩散速度的实验,两种气体扩散相遇时形成白色烟环.下列关于物质甲、乙的判断正确的是( )
已知气体的摩尔质量越小,扩散速度越快.如图所示为气体扩散速度的实验,两种气体扩散相遇时形成白色烟环.下列关于物质甲、乙的判断正确的是( )
 已知气体的摩尔质量越小,扩散速度越快.如图所示为气体扩散速度的实验,两种气体扩散相遇时形成白色烟环.下列关于物质甲、乙的判断正确的是( )
已知气体的摩尔质量越小,扩散速度越快.如图所示为气体扩散速度的实验,两种气体扩散相遇时形成白色烟环.下列关于物质甲、乙的判断正确的是( )| A. | 甲是浓氨水,乙是浓硫酸 | B. | 甲是浓氨水,乙是浓硝酸 | ||
| C. | 甲是浓盐酸,乙是浓氨水 | D. | 甲是浓硝酸,乙是浓氨水 |
12.同温同压下,下列各组热化学方程式中,△H1<△H2 的是( )
| A. | C(s)+$\frac{1}{2}$O2(g)═CO(g);△H1 C(s)+O2(g)═CO2(g);△H2 | |
| B. | $\frac{1}{2}$H2(g)+$\frac{1}{2}$Cl2(g)═HCl(g);△H1 H2(g)+Cl2(g)═2HCl(g);△H2 | |
| C. | 2H2(g)+O2(g)═2H2O(g);△H1 2H2(g)+O2(g)═2H2O(l);△H2 | |
| D. | S(g)+O2(g)═SO2(g);△H1 S(s)+O2(g)═SO2(g);△H2 |
19.下列说法正确的是( )
| A. | 将钠放入水中,钠将沉在水底 | |
| B. | 将一小块钠放在稀盐酸中,钠将与水反应生成NaOH和H2,生成的NaOH再与HCl反应生成NaCl和H2O | |
| C. | 将一小块钠放在CuSO4溶液中发生如下反应:2Na+CuSO4═Na2SO4+Cu | |
| D. | Na2O和Na2O2中,氧元素化合价不同 |
13.某溶液中可能含有Na+、I-、CO32-、SO32-、Br-、NH4+、Ba2+.某兴趣小组为确定该溶液的组成,进行了下列实验:取样,滴加足量氯水,有气泡产生,溶液呈橙色;向橙色溶液中加BaCl2溶液或淀粉均无明显变化.下列说法正确的是( )
| A. | 溶液中一定存在Na+、I-、CO32- | |
| B. | 溶液中一定不存在的只有I-、SO32- | |
| C. | 只需再进行一个实验,就可完全确定溶液的组成 | |
| D. | 溶液中一定存在Br-、CO32-,至少存在Na+、NH4+中的一种 |
14.如图为某固体溶解度随温度变化的曲线.该固体从溶液中析出时不带结晶水.M、N两点分别表示该固体形成的两份溶液在不同温度时的浓度.当条件改变时,溶液新的状态在图中对应的点的位置可能也随之变化,其中判断不正确的是( )

| A. | 加水稀释(假设温度都不变)时,M、N点均不动 | |
| B. | 都降温10℃后,M点沿曲线向左下移,N点向左平移 | |
| C. | 都升温10℃后,M、N点均向右平移 | |
| D. | 蒸发溶剂(假设温度都不变)时,先是M点不动,N点向上移至曲线;继续蒸发溶剂,M、N点都不动 |
 氯气是氯碱工业的主要产品之一,是一种常用的消毒剂,其消毒原理是与水反应生成了次氯酸:Cl2+H2O?HCl+HClO K=4.5×10-4
氯气是氯碱工业的主要产品之一,是一种常用的消毒剂,其消毒原理是与水反应生成了次氯酸:Cl2+H2O?HCl+HClO K=4.5×10-4 氯碱工业以电解精制饱和食盐水的方法制取氯气、氢气、烧碱和氯的含氧酸盐等系列化工产品.图2是离子交换膜法电解食盐水的示意图,图中的离子交换膜只允许阳离子通过.完成下列填空:
氯碱工业以电解精制饱和食盐水的方法制取氯气、氢气、烧碱和氯的含氧酸盐等系列化工产品.图2是离子交换膜法电解食盐水的示意图,图中的离子交换膜只允许阳离子通过.完成下列填空: