题目内容
【题目】按要求完成下列问题
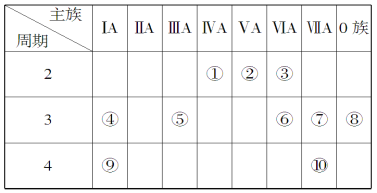
I.下列几种微粒或物质
①14C ②16O ③14N ④18O ⑤O2 ⑥O3
⑦CH3-CH3 ⑧C2H6 ⑨CH3- CH2-OH ⑩ CH3-O-CH3
(1)互为同位素的是______,(填序号,下同)质子数不同中子数相同的是______________
(2)互为同素异形体的是_________, 互为同分异构体的是_____________________
II.在25 C、101 kPa的条件下,

对于反应H2(g)+Cl2(g)= 2HCl(g), 测得生成2 mol HCI(g)时,反应过程中放出183 kJ的热量,则断开1 mol H- Cl键所需的能量是____ kJ.

III.如图所示的原电池装置中,正极的电极反应方程式是________________________
【答案】②④ ① ② ⑤ ⑥ ⑨ ⑩ 431 2H++2e-==H2 ↑
【解析】
I.具有相同质子数、不同中子数的原子为同位素;同种元素的不同单质,互为同素异形体;具有相同分子式、不同结构的有机物互为同分异构体;
II.根据焓变=反应物总键能-生成物总键能;
III.原电池装置中,正极氧化剂得电子发生还原反应。
I.(1)②16O④18O质子数均为8,中子数分别为8、10,故互为同位素的是②④,①14C②16O质子数不同分别为6、8,中子数相同均为8,质子数不同中子数相同的是① ②,故答案为:②④;① ②;
(2)⑤O2 ⑥O3是氧元素形成的两种单质,互为同素异形体的是⑤⑥,⑨CH3- CH2-OH ⑩ CH3-O-CH3 的分子式均为:C2H6O,前者是醇类,后者是醚类,互为同分异构体的是⑨ ⑩,故答案为:⑤⑥;⑨ ⑩;
II.根据焓变=反应物总键能-生成物总键能,断裂1molH-H键与1molCl-Cl键吸收的能量之和,即436kJ+243kJ=679kJ,设断开1molH-Cl键吸收的总能量为E(H-Cl),则有(436kJ+243kJ)-2×E(H-Cl)=-183kJ,则E(H-Cl)=431kJ,,故答案为:431;
III.原电池装置中,正极氧化剂得电子发生还原反应,氢离子得电子生成氢气,正极的电极反应方程式是2H++2e-==H2 ↑,故答案为:2H++2e-==H2 ↑。

 阅读快车系列答案
阅读快车系列答案