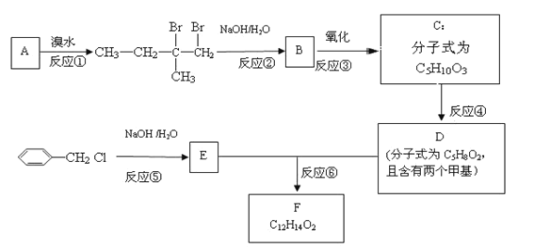
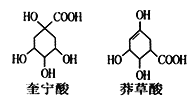
题目内容
【题目】已知酸性:![]() > H2CO3>
> H2CO3>![]() >HCO3-,综合考虑反应物的转化率和原料成本等因素,将
>HCO3-,综合考虑反应物的转化率和原料成本等因素,将 转变为
转变为 的最佳方法是
的最佳方法是
A. 与稀H2SO4共热后,加入足量的NaOH溶液
B. 与稀H2SO4共热后,加入足量的NaHCO3溶液
C. 与足量的NaOH溶液共热后,再通入足量CO2
D. 与足量的NaOH溶液共热后,再加入适量H2SO4
【答案】C
【解析】
酸性:![]() >H2CO3>
>H2CO3>![]() >HCO3-,
>HCO3-,![]() 转化为
转化为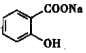 ,则羧基、酯基都发生变化但是酚羟基不能发生反应,据此分析解答。
,则羧基、酯基都发生变化但是酚羟基不能发生反应,据此分析解答。
A.先与稀硫酸反应生成邻羟基苯甲酸,再加入NaOH生成邻酚钠苯甲酸钠,不符合,故A错误;
B.与稀硫酸反应后生成邻羟基苯甲酸,再加入碳酸钠溶液,酚羟基和羧基都反应,不符合,故B错误;
C.与足量NaOH溶液反应后生成邻酚钠苯甲酸钠,然后通入足量二氧化碳生成邻羟基苯甲酸钠,故C正确;
D.与足量NaOH溶液反应后生成邻酚钠苯甲酸钠,然后加入稀硫酸生成邻羟基苯甲酸,不符合,故D错误;
故答案为C。

练习册系列答案
相关题目
【题目】根据下列实验操作和现象所得到的结论正确的是
选项 | 实验操作和现象 | 实验结论 |
A | 向NaHS溶液中加入盐酸产生大量气泡 | 氯的非金属性强于硫 |
B | 向溶液中加盐酸酸化的氯化钡溶液产生白色沉淀 | 原溶液中一定含 |
C | 将铁片和铜片用导线连接后插入浓硝酸,铁片表面产生气泡 | 铜的活泼性强于铁 |
D | 常温下测得CH3COONH4溶液pH=7 | 相同温度下CH3COOH和NH3·H2O电离常数相同 |
A.AB.BC.CD.D