题目内容
15.Cu2O是一种红色或黄色的粉末,在工业上可用作有机合成催化剂或电子工业材料等.(1)工业上可以用Na2SO3 还原CuSO4 的方法制备Cu2O,反应控制的温度为100℃~105℃,pH为3.5~5.5,其反应的化学方程式为2CuSO4+3Na2SO3═Cu2O+3Na2SO4+2SO2↑.也可以用电解法制备,电解时以铜作阳极,氢氧化钠为电解质溶液,写出电解时阳极发生的电极反应:2Cu-2e-+2OH-=Cu2O↓+H2O.
(2)某同学在实验室发现了一瓶使用过的红色粉末,且实验室中只有Fe2O3 和Cu2O两种颜色为红色的试剂,因此他就通过实验来探究该红色粉末的成分,已知Cu2O是一种碱性氧化物,溶于稀H2SO4生成Cu和CuSO4 ,在空气中加热生成CuO.
①请完成Cu2O与稀H2SO4反应的化学方程式:
Cu2O+H2SO4═Cu+CuSO4 +H2O;
②提出合理的假设:
假设1:红色粉末是Fe2O3 ;
假设2:红色粉末是Cu2O;
假设3:红色粉末是Fe2O3 和Cu2O的混合物.
③设计探究实验:
共选择的试剂:3mol•L-1 稀H2SO4、1mol•L-1 NaOH溶液、20%的KSCN溶液,3%的H2O2 溶液,稀HNO3、光亮的铁丝.
| 实验步骤 | 预期现象和结论 |
| 步骤1:取少量红色粉末于试管中,并加入过量3mol•L-1 稀H2SO4,充分反应后,将上层清液分成两份 | (1)若有红色固体剩余,则假设2,3可能成立; (2)若无红色固体剩余,则假设1,3可能成立 |
| 若步骤1中有红色固体剩余; 步骤2:取步骤1充分反应后的上层清液于试管中,加入足量3%的H2O2 溶液,再加入几滴20%的KSCN溶液 | 若溶液仍为蓝色,则假设2成立; |
| 若步骤1中有红色固体剩余; 步骤3:取步骤1充分反应后的上层清液于试管中,加入足量3%的H2O2 溶液,再加入几滴20%的KSCN溶液 | 若溶液变为血红色,则假设3成立. |
分析 (1)Na2SO3 还原CuSO4 生成Cu2O、Na2SO4和SO2;电解时以铜作阳极,铜在阳极放电生成Cu2O;
(2)①Cu2O与稀H2SO4反应生成Cu和CuSO4 ,方程式为Cu2O+H2SO4═Cu+CuSO4+H2O;
②根据题意,红色粉末可能是Fe2O3 ;也可能是Cu2O;还可能是二者的混合物;
③取步骤1充分反应后的上层清液于试管中,加入足量3%的H2O2 溶液,再加入几滴20%的KSCN溶液,若溶液仍为蓝色,说明溶液中只有Cu2+,则假设2成立;若溶液变为血红色,说明溶液中还含有Fe3+,则假设3成立.
解答 解:(1)Na2SO3 还原CuSO4 生成Cu2O、Na2SO4和SO2,反应的化学方程式为2CuSO4+3Na2SO3═Cu2O+3Na2SO4+2SO2↑;
电解时以铜作阳极,铜在阳极放电生成Cu2O,电极反应式为2Cu-2e-+2OH-=Cu2O↓+H2O;
故答案为:2CuSO4+3Na2SO3═Cu2O+3Na2SO4+2SO2↑;2Cu-2e-+2OH-=Cu2O↓+H2O;
(2)①Cu2O与稀H2SO4反应生成Cu和CuSO4 ,方程式为Cu2O+H2SO4═Cu+CuSO4+H2O;
故答案为:Cu2O+H2SO4═Cu+CuSO4+H2O;
②根据题意,红色粉末可能是Fe2O3 ;也可能是Cu2O;还可能是二者的混合物;
故答案为:红色粉末是Cu2O;
③取步骤1充分反应后的上层清液于试管中,加入足量3%的H2O2 溶液,再加入几滴20%的KSCN溶液,若溶液仍为蓝色,说明溶液中只有Cu2+,则假设2成立;若溶液变为血红色,说明溶液中还含有Fe3+,则假设3成立;
故答案为:
| 实验步骤 | 预期现象和结论 |
| 步骤1:取少量红色粉末于试管中,并加入过量3mol•L-1 稀H2SO4,充分反应后,将上层清液分成两份 | (1)若有红色固体剩余,则假设2,3可能成立; (2)若无红色固体剩余,则假设1,3可能成立 |
| 若步骤1中有红色固体剩余; 步骤2:取步骤1充分反应后的上层清液于试管中,加入足量3%的H2O2 溶液,再加入几滴20%的KSCN溶液 | 若溶液仍为蓝色,则假设2成立; |
| 若步骤1中有红色固体剩余; 步骤3:取步骤1充分反应后的上层清液于试管中,加入足量3%的H2O2 溶液,再加入几滴20%的KSCN溶液 | 若溶液变为血红色,则假设3成立. |
点评 本题考查较为综合,涉及氧化亚铜的制备方案、电解、红色物质的探究,侧重于学生的分析能力的考查,题目难度中等

 阅读快车系列答案
阅读快车系列答案 ,B、C可形成离子化合物B3C2.下列说法错误的是( )
,B、C可形成离子化合物B3C2.下列说法错误的是( )| A. | A元素在元素周期表中位于第三周期第IVA族 | |
| B. | B3C2中既含离子键又含共价键 | |
| C. | B的离子半径比C的离子半径小 | |
| D. | C的氢化物可与D的最高价氧化物的水化物反应生成盐 |
| A. | 一定相同 | B. | 一定不同 | C. | 可能不同 | D. | 无法确定 |
| A. | M的能量一定低于X的,N的能量一定低于Y的 | |
| B. | 因为该反应为吸热反应,故一定要加热反应才能进行 | |
| C. | 破坏反应物中化学键吸收的能量小于形成生成物中化学键所放出的能量 | |
| D. | M和N的总能量一定低于X和Y的总能量 |
| A. | 分子个数 | B. | 原子个数 | C. | 物质的质量 | D. | 物质的量 |
| A. | Na和Na+的化学性质相似 | |
| B. | 钠在空气中燃烧生成氧化钠 | |
| C. | 钠可与硫酸铜溶液反应得到铜 | |
| D. | 实验室通常把钠保存在石蜡油或煤油中 |
| A. | 常温下,10L pH=12的Na2CO3溶液中含有的OH-离子数目为0.1NA | |
| B. | 50mL 18.4 mol/L浓硫酸与足量铜加热反应,生成SO2分子的数目为0.46NA | |
| C. | 1mol羟基(-OH)中含电子数为10NA | |
| D. | 4.6g 金属钠与足量乙醇反应放出2.24L氢气 |
 某研究性学习小组根据氧化还原反应规律,欲探究NO2、NO与Na2O2反应的情况.
某研究性学习小组根据氧化还原反应规律,欲探究NO2、NO与Na2O2反应的情况.

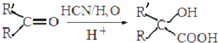
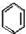 生成
生成 的反应类型是取代反应.
的反应类型是取代反应. .
. .
.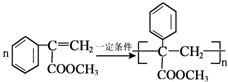 .
.