题目内容
【题目】某同学为确定某烃的分子式及其可能的结构简式,做了如下实验:标准状况下,取0.1mol某烃,在氧气中完全燃烧,生成的二氧化碳体积为22.4L,同时得到16.2g水。
(1)该烃的摩尔质量为______________。
(2)该烃的分子式为____________________。
(3)该烃有一种可能的结构为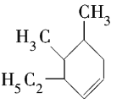 ,其系统命名为___________。
,其系统命名为___________。
(4) 属于______________(选填序号)。
属于______________(选填序号)。
a.环烃b.烷烃c.芳香烃d.不饱和烃
【答案】138g/mol C10H18 4,5-二甲基-3-乙基环己烯 ad
【解析】
根据标准状况下二氧化碳的体积计算二氧化碳的物质的量,利用水的质量计算水的物质的量,然后利用原子守恒计算其烃分子中含有的碳、氢原子个数,进而得到烃分子的分子式,结合题干中的问题分析解答。
(1)生成CO2物质的量为22.4L÷22.4L/mol=1mol,生成水的物质的量为16.2g÷18g/mol=0.9mol,即0.1mol该烃燃烧生成1molCO2、0.9molH2O,根据原子守恒可知烃分子含有10个碳原子和18个氢原子,所以其分子式为C10H18,则其摩尔质量是138g/mol;
(2)根据以上分析可知该烃的分子式为C10H18;
(3)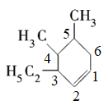 中含有1个碳碳双键和一个六元环,4,5号碳上各含有一个甲基,3号碳上含有一个乙基,故其名称为4,5-二甲基-3-乙基环己烯;
中含有1个碳碳双键和一个六元环,4,5号碳上各含有一个甲基,3号碳上含有一个乙基,故其名称为4,5-二甲基-3-乙基环己烯;
(4) 属于含有一个碳碳双键且含有一个环状结构,分子中只含有碳氢两种元素,属于环状烯烃,为不饱和烃,不含苯环,不属于芳香烃,答案选a、d。
属于含有一个碳碳双键且含有一个环状结构,分子中只含有碳氢两种元素,属于环状烯烃,为不饱和烃,不含苯环,不属于芳香烃,答案选a、d。

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目