��Ŀ����
20��ij��ѧ��ȤС������ͼ��ʾװ�ý���ʵ�飬̽������������Ӧ�IJ��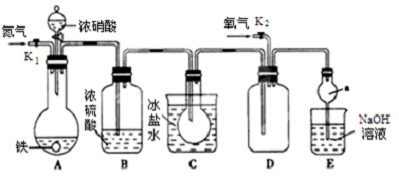
�������ϵ�֪��
����Ũ����ͻ��ý�����Ӧ�����У���������Ũ�ȵĽ��ͣ������ɵIJ�����+4��+2��-3�۵ȵ��Ļ����
����ʱ��NO2��N2O4ͬʱ���ڣ��ڵ���0��ʱ������ֻ����ɫ��N2O4�ľ�����ڣ�
��ش��������⣺
��1��װ���и�����װ���Լ���������������IJ���˳��ΪCADB��
A��ͨ��N2 B������ŨHNO3 C������K1 D���رջ���K1
��2��װ��A�У�����Ũ�������ǰû�����������ԭ���dz���ʱ������Ũ�����γ���������Ĥ����ֹ��Ӧ��һ��������
��3����Ӧ������װ��D�еĻ���K2����ͨ������������ȫ�ܽ���Ũ��������ɵ�NO2�����к���NO������ΪDƿ����������ɫ��Ϊ����ɫ��װ��D�з����ķ�Ӧ�Ļ�ѧ����ʽΪ2NO+O2�T2NO2��
��4��Cװ�õ������ǰ�NO2ȫ��ת��ΪN2O4���壬������Dװ���ж�NO����֤�������ţ�
��5����Ӧֹͣ��װ��A������ʣ�࣮֤��װ��A����Һ���Ƿ���Fe2+��ѡ���ҩƷ��c��������ţ�
a������ b����ˮ c��KMnO4��Һ d�����軯����Һ
��6�������Ƿ�����-3�۵��Ļ����Ӧ���е�ʵ���������������ȡ������Ӧ��A����Һ���Թ��У������м���ŨNaOH��Һ�����ȣ���ʪ��ĺ�ɫʯ����ֽ�ӽ��Թܿڣ�����ֽ��������A������NH4+��
���� ʵ�鿪ʼǰҪ�ȴ�A���ֵĻ���K1������ͨһ��ʱ��ĵ����ٹر�K1���ž�װ���еĿ���������Ũ���ᷴӦ���ɶ���������һ���������壬�����ͨ��װ��C���ڵ���0��ʱ����ֻ����ɫ��N2O4������ڣ�A�еķ�Ӧֹͣ��D�еĻ���K2����ͨ������������Ӧȷ��NO��������D�г��ֺ���ɫ���壬˵����һ�������������ɣ�ʣ������������������Һ���գ�
��1����������������Ӧ������NO������NO�ױ������е��������������Ը�����װ���Լ���Ӧ��ͨ������װ���еĿ�����
��2�����ݳ���������Ũ�����з����ۻ�����������ʱ������Ũ�����γ���������Ĥ����ֹ��Ӧ��һ��������
��3��NO�������������ɺ���ɫ�������������
��4����NO2ȫ��ת��ΪN2O4���壬��ֹ������������NO�ļ��飻
��5�������������ӵ��Լ�ΪKMnO4��Һ���������ӱ�KMnO4��Һ������ʹKMnO4��Һ��ɫ��
��6������-3�۵��Ļ��������ɣ�Ӧ����NH4+������A��Һ���Ƿ���NH4+���Ӽ��ɣ�
��� �⣺ʵ�鿪ʼǰҪ�ȴ�A���ֵĻ���K1������ͨһ��ʱ��ĵ����ٹر�K1���ž�װ���еĿ���������Ũ���ᷴӦ���ɶ���������һ���������壬�����ͨ��װ��C���ڵ���0��ʱ����ֻ����ɫ��N2O4������ڣ�A�еķ�Ӧֹͣ��D�еĻ���K2����ͨ������������Ӧȷ��NO��������D�г��ֺ���ɫ���壬˵����һ�������������ɣ�ʣ������������������Һ���գ�
��1����Ϊ����������Ӧ����������Ũ�ȵĽ��ͣ������ɵIJ�����+4��+2��-3�۵ȵ��Ļ�����������NO������NO�ױ������е��������������Ը�����װ���Լ���Ӧ��ͨ������װ���еĿ���������������IJ���˳��Ϊ����K1��ͨ��N2�ž�װ���еĿ����ٹرջ���K1������ٵ���ŨHNO3������Ӧ���ʴ�Ϊ��CADB��
��2������ʱ������Ũ���ᷴӦ����һ�����ܵ������ﱡĤ����ֹ������Ũ�����һ����Ӧ���������ۻ��������Ե���Ũ�������ǰû����������
�ʴ�Ϊ������ʱ������Ũ�����γ���������Ĥ����ֹ��Ӧ��һ��������
��3����ɫ��NO�������������ɺ���ɫ���������������Ӧ����ʽΪ2NO+O2=2NO2���ʴ�Ϊ��Dƿ����������ɫ��Ϊ����ɫ��2NO+O2=2NO2��
��4�������¶ȣ�������������ȫת��ΪN2O4���壬��ֹ����������NO����ĸ��ţ��ʴ�Ϊ����NO2ȫ��ת��ΪN2O4���壬������Dװ���ж�NO����֤�������ţ�
��5����Ϊ�������Ӿ���ǿ��ԭ�ԣ��������������ױ�KMnO4��Һ������ʹKMnO4��Һ��ɫ���ʴ�Ϊ��c��
��6������-3�۵��Ļ������ǰ�����������������ˮ���ɰ�ˮ����ˮ��������笠����ӣ�����笠����ӵķ����ǣ�ȡ������Ӧ��A����Һ���Թ��У������м���ŨNaOH��Һ�����ȣ���ʪ��ĺ�ɫʯ����ֽ�ӽ��Թܿڣ�����ֽ��������A������NH4+��
�ʴ�Ϊ��ȡ������Ӧ��A����Һ���Թ��У������м���ŨNaOH��Һ�����ȣ���ʪ��ĺ�ɫʯ����ֽ�ӽ��Թܿڣ�����ֽ��������A������NH4+��
���� ���⿼��������������ʣ�笠����ӡ��������ӵļ����Ǹ߿��ȵ㣬ע�⣺����ʱ������Ũ����Dz���Ӧ�����Ƿ����˶ۻ�������ֹ�˽�һ����Ӧ��Ϊ�״��㣬��Ŀ�Ѷ��еȣ�

| A�� | �Ҵ��Ͷ����ѻ�Ϊͬ���칹�壬���ú��������˴Ź����������ɼ������� | |
| B�� | �����Ӳ֬�ụΪͬϵ�C2H4��C18H38Ҳ��Ϊͬϵ�� | |
| C�� | �л���W�� ������ˮ����ﶼ���Է�����ȥ��Ӧ ������ˮ����ﶼ���Է�����ȥ��Ӧ | |
| D�� | ��ϩ�ļӳɷ�Ӧ��������KMnO4��Һ���ã������������̼̼˫���й� |
| A�� | CO��CO2��Ϊ���������� | B�� | CO��ú������Ҫ�ɷ�֮һ | ||
| C�� | CO2��������� | D�� | ����CO2���ŷſɵ���������γ� |
| A�� | pH��7����Һ�У�S${{O}_{4}}^{2-}$��C${{O}_{3}}^{2-}$��Na+��K+ | |
| B�� | ʹ��̪���ɫ����Һ�У�Na+��K+��Cl-��CH3COO- | |
| C�� | 0.1 mol•L-1 NH4Al��SO4��2��Һ�У�Al${{O}_{2}}^{-}$��Mg2+��Cl-��S${{O}_{4}}^{2-}$ | |
| D�� | $\frac{{c��H}^{+}��}{{c��OH}^{-}��}$=1012����Һ�У�Na+��Ba2+��N${{O}_{3}}^{-}$��ClO- |
 �����£���0.10mol•L-1����ֱ�ζ�20.00mL 0.10mol•L-1����������Һ�Ͱ�ˮ���ζ���������ҺpH������������[V��HCl��]�ı仯��ϵ��ͼ��ʾ������˵������ȷ���ǣ�������
�����£���0.10mol•L-1����ֱ�ζ�20.00mL 0.10mol•L-1����������Һ�Ͱ�ˮ���ζ���������ҺpH������������[V��HCl��]�ı仯��ϵ��ͼ��ʾ������˵������ȷ���ǣ�������| A�� | ���ʾ���ǵζ���ˮ�����ߣ���V��HCI��=20 mLʱ���У�c��Cl-����c��N${{H}_{4}}^{+}$����c��H+����c��OH-�� | |
| B�� | ��pH=7ʱ���ζ���ˮ���ĵ�V��HCl��=20 mL����c��N${{H}_{4}}^{+}$��=c��Cl-�� | |
| C�� | �ζ�����������Һʱ����V��HCl����20 mL����һ���У�c��Cl-����c��Na+����c��H+����c��OH-�� | |
| D�� | ���ζ���ˮ����V��HCl��=10 mLʱ���У�2[c��OH-��-c��H+��]=c��N${{H}_{4}}^{+}$��-c��NH3•H2O�� |
| A�� | AgI��AgCl��ˮ��Ϻ��γɵķ�ɢϵ�У�c��Ag+��=c��I-����c��C1-�� | |
| B�� | 25��ʱ����pH��ȵ�NH4C1��Һ�������У�ˮ�ĵ���̶�Ҳ��� | |
| C�� | 25��ʱ����pH=11��NaOH��Һ��pH=3��ij����HA����Һ�������ϣ���Ϻ����Һ�ʼ��� | |
| D�� | 25��ʱ����pH=2��H2C2O4 ��һ�ֶ�Ԫ���ᣩ��Һ��pH=12��NaOH��Һ�����������Ϻ��γɵ���Һ�У�һ�����ڣ�c��Na+��+c��H+��=c��OH-��+c��HC2O4-��+2c��C2O42-�� |
| A�� | 166 | B�� | 99 | C�� | 67 | D�� | 32 |

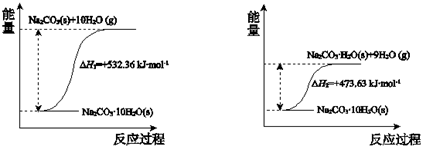

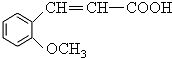 ��
�� ��
�� ��
��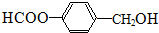 ����дһ�֣���
����дһ�֣���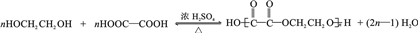 ��
�� Ϊԭ����
Ϊԭ���� �ĺϳ�·������ͼ�����Լ����ã����ڷ����������Ӧ�����ʣ���������ע����Ӧ�������ϳ�·������ͼʾ����ͼ2��
�ĺϳ�·������ͼ�����Լ����ã����ڷ����������Ӧ�����ʣ���������ע����Ӧ�������ϳ�·������ͼʾ����ͼ2��