题目内容
16.关于NO的下列叙述,不正确的是( )| A. | NO可以是某些含低价氮物质的氧化产物 | |
| B. | NO可以是某些含高价氮物质的还原产物 | |
| C. | 已知亚硝酸钠的化学式是NaNO2,则NO不是亚硝酸酐 | |
| D. | NO2和NO都是红棕色气体 |
分析 A、NO中N元素的化合价为+2价,具有还原性,某些含高价N物质还原可生成NO;
B、氮元素化合价可以从高价态降低为+2价被还原;
C、酸酐是指对应中心元素化合价形成的氧化物,亚硝酸中N元素的化合价为+3价,NO中氮元素的化合价为+2价,不是亚硝酸酐;
D、NO是无色气体.
解答 解:A.NO中N元素的化合价为+2价,具有还原性,可以为低价氧化物的氧化产物,如NH3被氧化为NO,故A正确;
B.NO为低价氧化物,某些含高价N物质还原可生成NO,如稀硝酸中氮元素+5价变化为+2价,故B正确;
C.亚硝酸中N元素的化合价为+3价,酸酐为N2O3,NO不是亚硝酸酐,故C正确;
D.NO2是红棕色气体,NO为无色气体,故D错误.
故选D.
点评 本题考查了一氧化氮的性质,明确一氧化氮中氮元素的化合价以及与其它含氮物质的相互转化是解答关键,题目难度不大.

练习册系列答案
相关题目
7.下列各项中表达正确的是( )
| A. | NH3分子的电子式: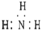 | B. | CH4分子的比例模型: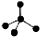 | ||
| C. | O原子的结构示意图: | D. | N2的结构式:N≡N |
11.为方便某些计算,有人将98%的浓硫酸表示成下列形式,其中合理的是( )
| A. | H2SO4•H2O | B. | H2SO4•SO3 | C. | H2SO4•$\frac{1}{9}$H2O | D. | SO3•$\frac{10}{9}$H2O |

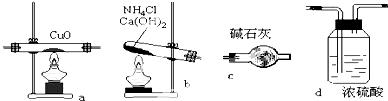 实验室用氨气在加热下还原氧化铜的方法铜的相对原子质量如果选用测定反应物氧化铜和生成物水的质量[m(CO)、m(H2O)]时,如图所示请用下列仪器设计一个简单实验方案.
实验室用氨气在加热下还原氧化铜的方法铜的相对原子质量如果选用测定反应物氧化铜和生成物水的质量[m(CO)、m(H2O)]时,如图所示请用下列仪器设计一个简单实验方案.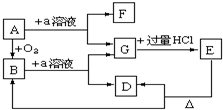 在下列物质的转化关系中,A是一种固体单质,E是一种白色沉淀,F是最轻的气体单质,据此填写下列空白:
在下列物质的转化关系中,A是一种固体单质,E是一种白色沉淀,F是最轻的气体单质,据此填写下列空白: