题目内容
10.已知反应:①2C(s)+O2(g)=2CO(g)△H=-221kJ/mol,②稀溶液中,H+(aq)+OH-(aq)=H2O(l)△H=-57.3kJ/mol,反应热要有正负号,中和热不用,弱酸的中和热减少,下列结论正确的是( )| A. | 碳的燃烧热大于110.5 kJ/mol | |
| B. | ①的反应热为221 kJ/mol | |
| C. | 稀硫酸与稀NaOH溶液反应的中和热为57.3 kJ/mol | |
| D. | 稀醋酸与稀NaOH溶液反应生成1 mol水,放出57.3 kJ 热量 |
分析 A、CO燃烧生成二氧化碳继续放出热量;
B、反应热包含符号,①的反应热为-221 kJ•mol-1;
C、中和热为强酸与强碱在稀溶液中反应生成1 mol水放出的热量;
D、醋酸是弱电解质,电离需吸收热量.
解答 解:A、由反应①可知,1mol碳燃烧生成CO放出的热量为110.5 kJ,CO燃烧生成二氧化碳继续放出热量,故1mol碳完全燃烧放出的热量大于110.5 kJ,所以碳的燃烧热大于110.5 kJ/mol,故A正确;
B、反应热包含符号,①的反应热为-221 kJ•mol-1,故B错误;
C、中和热为强酸与强碱在稀溶液中反应生成1 mol水放出的热量,故C错误;
D、醋酸是弱电解质,电离需吸收热量,稀醋酸与稀NaOH溶液反应生成1mol水△,放出的热量小于57.3 kJ,故D错误;
故选A.
点评 本题考查学生对于反应热、中和热的理解及有关计算等,难度不大,注意稀的强酸、强碱的中和热为△H=-57.3kJ/mol.

练习册系列答案
 云南师大附小一线名师提优作业系列答案
云南师大附小一线名师提优作业系列答案 冲刺100分单元优化练考卷系列答案
冲刺100分单元优化练考卷系列答案
相关题目
20.常温下时,有pH=3的盐酸和醋酸溶液,下列说法正确的是( )
| A. | 两种溶液中由水电离出来的c(H+)不相同 | |
| B. | 中和相同体积的两种酸溶液所需NaOH的物质的量相同 | |
| C. | 分别用蒸馏水稀释m倍和n倍,若两溶液pH仍相同,则m>n | |
| D. | 将两溶液等体积混合,则c(H+)>c(CH3COO-)═c(Cl-)>c(OH-) |
5.室温下,向pH=13的氢氧化钡溶液中加入等体积的下列溶液后,滴入石蕊试液,出现蓝色,该溶液可能是( )
| A. | 0.05 mol•L-1的硫酸溶液 | B. | 0.1 mol•L-1的硫酸钠溶液 | ||
| C. | pH=1的醋酸溶液 | D. | pH=1的盐酸 |
15.某化学反应的能量变化如图所示.下列有关叙述正确的是( )
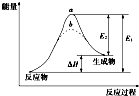

| A. | 逆反应的活化能小于正反应的活化能 | |
| B. | a、b分别对应有催化剂和无催化剂的能量变化 | |
| C. | 该反应的反应热△H=E2-E1 | |
| D. | 催化剂能改变反应的焓变 |
19.铜镁合金1.52g完全溶解于50mL密度为1.40g•mL-1、质量分数为63%的浓硝酸中,得到NO2和N2O4的混合气体1120mL(标准状况).向反应后的溶液中加入1.0mol•L-1 NaOH溶液,当金属离子全部沉淀时,得到2.54g沉淀.下列说法不正确的是( )
| A. | 得到2.54 g沉淀时,加入NaOH溶液的体积是600 mL | |
| B. | 该浓硝酸中HNO3的物质的量浓度是14.0 mol•L-1 | |
| C. | 该合金中铜与镁的物质的量之比是2:1 | |
| D. | NO2和N2O4的混合气体中,NO2的体积分数是80% |
20.下列各组变化中,后者一定包括前者的是( )
| A. | 物理变化、化学变化 | B. | 氧化还原反应、分复反应 | ||
| C. | 氧化还原反应、化合反应 | D. | 分解反应、复分解反应 |
