题目内容
2.在元素周期表中,最外层只有1个未成对电子的主族元素原子处于ⅠA、ⅢA、ⅦA族;最外层有2个未成对电子的主族元素原子处于ⅣA、ⅥA族.分析 在元素周期表中,最外层只有1个未成对电子的主族元素原子最外层电子数可分别为1、3、7,最外层有2个未成对电子的主族元素原子最外层电子数分别为4、6.
解答 解:在元素周期表中,最外层只有1个未成对电子的主族元素原子最外层电子数可分别为1、3、7,为ⅠA、ⅢA、ⅦA族元素,最外层有2个未成对电子的主族元素原子最外层电子数分别为4、6,为ⅣA、ⅥA族元素,
故答案为:ⅠA、ⅢA、ⅦA;ⅣA、ⅥA.
点评 本题综合考查原子核外电子排布以及原子结构与元素周期表知识,侧重于基础知识的考查,为高考高频考点,注意相关基础知识的积累,难度不大.

练习册系列答案
相关题目
13.用托盘天平(指针向上的)称量样品时,若指针偏向右边,则表示( )
| A. | 左盘重,样品轻 | B. | 左盘轻,砝码重 | C. | 右盘重,砝码轻 | D. | 右盘轻重,样品重 |
10.已知反应:①2C(s)+O2(g)=2CO(g)△H=-221kJ/mol,②稀溶液中,H+(aq)+OH-(aq)=H2O(l)△H=-57.3kJ/mol,反应热要有正负号,中和热不用,弱酸的中和热减少,下列结论正确的是( )
| A. | 碳的燃烧热大于110.5 kJ/mol | |
| B. | ①的反应热为221 kJ/mol | |
| C. | 稀硫酸与稀NaOH溶液反应的中和热为57.3 kJ/mol | |
| D. | 稀醋酸与稀NaOH溶液反应生成1 mol水,放出57.3 kJ 热量 |
17.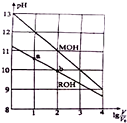 常温下,浓度均为0.10mol/L、体积均为V0的MOH和ROH溶液,分别加水稀释至体积V,pH随lg$\frac{V}{{V}_{0}}$的变化如图所示,下列叙述错误的是( )
常温下,浓度均为0.10mol/L、体积均为V0的MOH和ROH溶液,分别加水稀释至体积V,pH随lg$\frac{V}{{V}_{0}}$的变化如图所示,下列叙述错误的是( )
 常温下,浓度均为0.10mol/L、体积均为V0的MOH和ROH溶液,分别加水稀释至体积V,pH随lg$\frac{V}{{V}_{0}}$的变化如图所示,下列叙述错误的是( )
常温下,浓度均为0.10mol/L、体积均为V0的MOH和ROH溶液,分别加水稀释至体积V,pH随lg$\frac{V}{{V}_{0}}$的变化如图所示,下列叙述错误的是( )| A. | MOH的碱性强于ROH的碱性 | |
| B. | ROH的电离程度:b点大于a点 | |
| C. | 若两溶液无限稀释,则它们的c(OH-)相等 | |
| D. | 当lg$\frac{V}{{V}_{0}}$=2时,若两溶液同时升高温度,则$\frac{c({M}^{+})}{c({R}^{+})}$不变 |
7.已知氨水的密度随浓度的减小而增大,现将50g浓度为cmol•L-1,密度为ρg•cm-3的氨水中加入一定量的水稀释成0.5cmol•L-1,则加入水的体积为( )
| A. | 小于50mL | B. | 等于50mL | C. | 大于50mL | D. | 等于50/ρmL |
14.下列反应的离子方程式书写正确的是( )
| A. | 1.0 mol.L-l的NaAl02溶液和2.5 mol.L-l的盐酸等体积混合:2AlO${\;}_{2}^{-}$+5H+═Al(OH)3↓+Al3++H2O | |
| B. | 铜溶于0.5 mol.L-1的硝酸中:Cu+4H++2NO${\;}_{3}^{-}$═Cu2++2NO2↑+2H2O | |
| C. | 工业上将Cl2通人石灰乳中制漂白粉:Cl2+2OH-═Cl-+ClO-+H2O | |
| D. | 向Ba(OH)2溶液中加入少量的NH4HSO4溶液:Ba2++OH-+H++Si${\;}_{4}^{2-}$═BaSO4↓+H2O |