题目内容
20.设NA为阿伏加德罗常数的值,下列说法正确的是( )| A. | 标准状况下,11.2 L H2O中含有的分子数为0.5 NA | |
| B. | 把40 g NaOH固体溶于1 L水中,所得溶液中NaOH的物质的量浓度为1 mol•L-1 | |
| C. | 常温常压下,16g O3中含有NA个氧原子 | |
| D. | 1 mol钠原子中含有的电子数为NA |
分析 A、标况下,水为液体;
B、将氢氧化钠固体溶于1L水中,溶于体积大于1L;
C、臭氧由氧原子构成;
D、钠原子中含11个电子.
解答 解:A、标况下,水为液体,故不能根据气体摩尔体积来计算其物质的量,故A错误;
B、将氢氧化钠固体溶于1L水中,溶于体积大于1L,故所得溶液的浓度小于1mol/L,故B错误;
C、臭氧由氧原子构成,故16g臭氧中含有的氧原子的物质的量n=$\frac{16g}{16g/mol}$=1mol,个数为NA个,故C正确;
D、钠原子中含11个电子,故1mol钠原子中含11mol电子即11NA个,故D错误.
故选C.
点评 本题考查了阿伏伽德罗常数的有关计算,掌握物质的量的计算公式和物质结构是解题关键,难度不大.

练习册系列答案
相关题目
10.下列叙述正确的是( )
| A. | 1摩尔任何物质都含有6.02×1023个分子 | |
| B. | 摩尔是国际单位制中7个基本物理量之一 | |
| C. | 含有6.02×1023个氧原子的H3PO4的物质的量是0.25mol | |
| D. | 氧气的摩尔质量等于它的相对原子质量 |
8.对于可逆反应2SO2+O$\frac{\underline{\;催化剂\;}}{△}$2SO3,在混合气体中充入一定量18O2,足够长的时间后,18O原子( )
| A. | 只存在于O2中 | B. | 只存在于SO3和O2中 | ||
| C. | 只存在于SO2和O2中 | D. | 存在于SO2、SO3和O2中 |
5.下列各组离子一定能大量共存的是( )
| A. | 在pH=1的溶液中:Na+、NO3-、I-、K+ | |
| B. | 常温下pH=7的溶液中:Fe3+、Mg2+、SO42-、Cl- | |
| C. | 常温下水电离的c(OH-)=1×10-13mol•L-1的溶液中:NH4+、HCO3-、SO42-、Cl- | |
| D. | 含有HCO3-的溶液中:K+、NH4+、NO3-、Ca2+ |
9.火法炼铜首先要焙烧黄铜矿,其反应为:2CuFeS2+O2═Cu2S+2FeS+SO2.下列说法正确的是( )
| A. | CuFeS2仅作还原剂,硫元素被氧化 | |
| B. | 每生成1molSO2,反应共转移6mol电子 | |
| C. | CuFeS2中被氧化的原子和被还原的原子数目之比为2:1 | |
| D. | 该反应中有两种物质作还原剂 |
 ,反应A的热化学方程式是4HCl(g)+O2(g)?2Cl2(g)+2H2O(g)△H=-115.6 KJ/mol.
,反应A的热化学方程式是4HCl(g)+O2(g)?2Cl2(g)+2H2O(g)△H=-115.6 KJ/mol.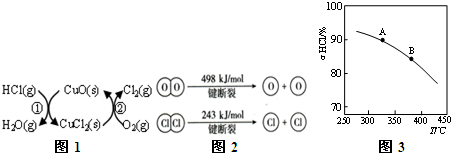
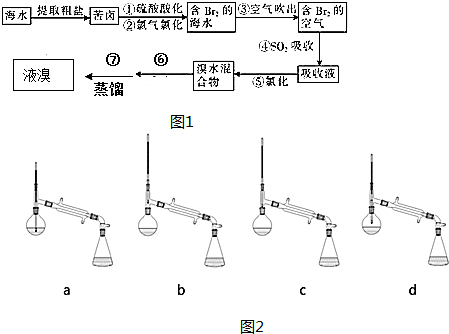
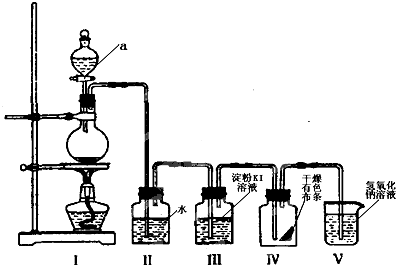
 ,在该反应中,当有0.1mol电子发生转移时,生成标准状况氯气的体积为1.12L.
,在该反应中,当有0.1mol电子发生转移时,生成标准状况氯气的体积为1.12L.