题目内容
(1)钢铁工业对促进经济和社会发展起了重要作用。
①不锈钢含有的Cr元素是在炼钢过程的氧吹 (填“前”或“后”)加入。
②炼钢时,加入硅、锰和铝的目的是 。
③炼铁和炼钢生产中,尾气均含有的主要污染物是 。从环保和经济角度考虑,上述尾气经处理可用作 。
(2)纯碱是一种重要的化工原料。目前制碱工业主要有“氨碱法”和“联合制碱法”两种工艺。
①“氨碱法”产生大量CaCl2废弃物,写出该工艺中产生CaCl2的化学方程式: ;
②写出“联合制碱法”有关反应的化学方程式: ;
③CO2是制碱工业的重要原料,“联合制碱法”与“氨碱法”中CO2的来源有何不同? 。
(1)①后(1分)②脱氧和调整钢的成分(2分)③ CO (2分) 燃料(或还原剂)(2分)(2)① 2NH4Cl+Ca(OH)2 2NH3↑+CaCl2+2H2O (2分)
2NH3↑+CaCl2+2H2O (2分)
② NH3+CO2+H2O+NaCl(饱和)=NaHCO3↓+NH4Cl (2分)
2NaHCO3 Na2CO3+CO2↑+H2O (2分)
Na2CO3+CO2↑+H2O (2分)
(或写总反应方程式:2NaCl+2NH3+CO2+H2O=Na2CO3+2NH4Cl)
③“氨碱法”CO2来源于灰石煅烧,“联合制碱法”CO2来源于合成氨工业的废气;(2分)
解析试题分析:(1)①因为Cr易被氧化,若氧吹前加入Cr会形成炉渣被除去;②加入硅、锰和铝的目的是脱氧和调整钢的成分③主要污染物是CO,故可用作燃料或还原剂;(2)“氨碱法”需要先制取氨气,故氯化钙来源于2NH4Cl+Ca(OH)2 2NH3↑+CaCl2+2H2O;②联合制碱法是先向氯化钠的饱和溶液中通入氨气,再通过二氧化碳制得碳酸氢钠晶体,过滤出来加热得碳酸钠;③“氨碱法”CO2来源于石灰石煅烧,“联合制碱法”CO2来源于合成氨工业的废气。
2NH3↑+CaCl2+2H2O;②联合制碱法是先向氯化钠的饱和溶液中通入氨气,再通过二氧化碳制得碳酸氢钠晶体,过滤出来加热得碳酸钠;③“氨碱法”CO2来源于石灰石煅烧,“联合制碱法”CO2来源于合成氨工业的废气。
考点:考查炼钢的过程和制碱的原理

 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案海洋中有丰富的食品、矿产、能源、药物和水产资源,下图为海水利用的部分过程。
下列有关说法正确的是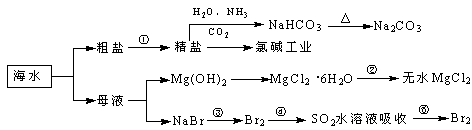
| A.过程①中除去粗盐中的SO42-、Ca2+、Mg2+、Fe3+等杂质,加入的药品顺序为:Na2CO3溶液→NaOH溶液→BaCl2溶液→过滤后加盐酸 |
| B.用澄清的石灰水可鉴别NaHCO3和Na2CO3 |
| C.过程②中结晶出的MgCl2·6H2O要在HCl氛围中加热脱水制得无水MgCl2 |
| D.工业上通过电解饱和MgCl2溶液制取金属镁 |
海水是一个巨大的化学资源库,下列有关海水综合利用的说法正确的是
| A.海水中含有溴元素,只需经过物理变化就可以得到溴单质 |
| B.海水蒸发制海盐的过程中只发生了化学变化 |
| C.从海水中可以得到MgCl2,电解熔融MgCl2可制备Mg |
| D.利用潮汐发电是将化学能转化为电能 |
[化学—选修2化学与技术](15分)
(1)下列关于工业生产说法正确的是 。(填序号)
| A.在侯氏制碱工业中,向饱和氯化钠溶液中先通二氧化碳,后通氨气 |
| B.在硫酸工业、合成氨工业、硝酸工业中,皆采用循环操作提高原料利用率 |
| C.在氯碱工业,电解槽被离子交换膜隔成阴极室和阳极室 |
| D.工业上采用电解熔融氯化铝的方法制取金属铝 |
(2)我国规定饮用水质量标准规定必须符合下表中要求:
| pH | Ca2+ 、Mg2+总浓度 | 细菌总数 |
| 6.5~8.5 | < 0.004 5 mol·L-1? | <100个·mL-1? |

①原水中含Ca2+ 、Mg2+ 、HCO3-、Cl-等,加入石灰生成Ca(OH)2,进而发生若干复分解反应,写出其中的离子方程式(只要求写出两个): ; 。
②FeSO4·7H2O是常用的凝聚剂,它在水中最终生成 沉淀;通入二氧化碳的目的是 和 。
③气体A的作用是 ,通常可以用Ca(ClO)2替代A,下列物质中 同样可以作为气体A的代用品(填编号,多选倒扣)。
a.ClO2 b.浓氨水 c.K2FeO4 d.SO2
(11分)从海水中可以获得淡水、食盐,并可提取镁和溴等物质。
(一)海水淡化的方法主要有 (只填一种)。
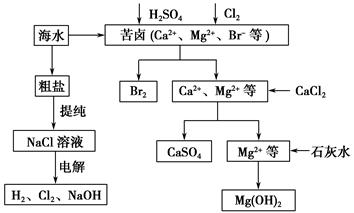
(二)从海水中提取溴和镁的流程如下图所示:
(1)提取Br2时,第一次通入Cl2后发生反应的离子方程式是 ;
②中SO2表现 (填“氧化”或“还原”)性;
第二次通入Cl2后,要提取Br2还要进行的操作为 。
(2)为了实现对镁离子的富集,①中加入的足量试剂是 (填化学式);
请从节约能源,提高金属镁的纯度分析,以下最适宜的冶炼的方法是
(填字母)。
A.Mg(OH)2 MgO MgO  Mg Mg |
B.Mg(OH)2  MgO MgO  Mg Mg |
C.Mg(OH)2 无水MgCl2 无水MgCl2 Mg Mg |
D.Mg(OH)2 MgCl2(溶液) MgCl2(溶液) Mg Mg |





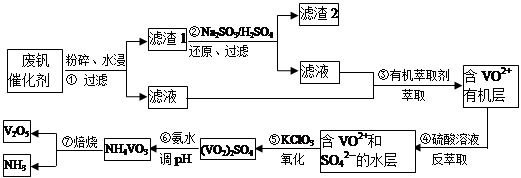
 VOA2(有机层)+ H2SO4(水层),则步骤④中可选择硫酸作反萃取的原因是_____________。
VOA2(有机层)+ H2SO4(水层),则步骤④中可选择硫酸作反萃取的原因是_____________。