题目内容
【题目】根据要求计算。
(1)0.5mol NaAlO2含有___mol Na+;_____mol AlO2-;含___个O。
(2)在100 mL 0.2 mol/L NaOH溶液中含溶质的物质的量___mol;配制50 mL 0.2 mol/LFeSO4溶液,需要FeSO4____ g。
(3)1.06 g的Na2CO3的物质的量是___mol;含有的CO32-离子数是___个。
(4)标准状况下,0.3 mol CH4的体积是___;含有碳原子质量是___;含有氢原子物质的量_____。
【答案】0.5 0.5 NA 0.02 1.52 0.01 0.01NA 6.72L 3.6g 1.2mol
【解析】
利用n=c×V=![]() =
=![]() 及微粒的结构进行计算。
及微粒的结构进行计算。
(1)一个NaAlO2中含有1个Na+,1个AlO2-,2个O,则0.5mol NaAlO2含有0.5mol Na+;0.5mol AlO2-;含0.5×2×NA= NA个O;
(2)n=c×V=0.2mol/L×0.1L=0.02mol;m= c×V×M=0.2mol/L×0.05L×152g/mol=1.52g;
(3)n=![]() =
=![]() =0.01mol;一个Na2CO3中含有1个CO32-,0.01molNa2CO3中含有0.01 NA个CO32-;
=0.01mol;一个Na2CO3中含有1个CO32-,0.01molNa2CO3中含有0.01 NA个CO32-;
(4)标准状况下,0.3 mol CH4的体积=n×Vm=0.3mol×22.4L/mol=6.72L;含有碳原子质量=n×M=0.3mol×12g/mol=3.6g;一个分子中含有4个氢原子,则氢原子物质的量=0.3 mol×4=1.2mol。

 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
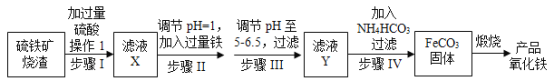
小学生10分钟应用题系列答案【题目】完成下列实验所选择的装置或仪器(夹持装置已略去)正确的是( )
选项 | A | B | C | D |
实验 | 用CCl4提取溴水中的Br2 | 从食盐水中提取NaCl固体 | 从KI和I2的固体混合物中回收I2 | 配制100 mL0.1000 mol·L-1Na2CO3溶液 |
装置或仪器 |
|
|
|
|
A.AB.BC.CD.D