题目内容
【题目】阿伏加德罗常数的近似值为6.02×1023。按要求完成下列填空:
(1)1molCl2中约含有___个氯气分子,约含有__个氯原子。含有6.02×1023个氢原子的H2SO4的物质的量是___;
(2)某硫酸钠溶液中含有3.01×1023个Na+,则该溶液中SO42-的物质的量是___。
(3)2L1mol/LMgCl2中镁离子的物质的量为___,Cl-的物质的量浓度为___。
(4)三种盐的混合溶液中含有0.2molNa+、0.25molMg2+、0.4molCl-、SO42-,则SO42-的微粒个数约为___。
【答案】NA 2NA 0.5mol 0.25mol 2mol 2mol/L 0.15NA
【解析】
(1)根据n=![]() ,结合分子的构成计算;
,结合分子的构成计算;
(2)根据n=![]() 计算n(Na+),由化学式可知n(SO42-)=
计算n(Na+),由化学式可知n(SO42-)=![]() n(Na+);
n(Na+);
(3)根据c=![]() 结合物质的分子式来计算;
结合物质的分子式来计算;
(4)溶液中阴离子和阳离子的正负电荷守恒,根据守恒思想来计算。
(1)根据n=![]() ,1molCl2中含有NA个氯气分子,含有2NA个氯原子,含有6.02×1023个氢原子的H2SO4的个数为
,1molCl2中含有NA个氯气分子,含有2NA个氯原子,含有6.02×1023个氢原子的H2SO4的个数为![]() ×6.02×1023,H2SO4的物质的量是0.5mol;
×6.02×1023,H2SO4的物质的量是0.5mol;
(2)n(Na+)=![]() =0.5mol,由化学式可知n(SO42-)=
=0.5mol,由化学式可知n(SO42-)=![]() n(Na+)=0.5mol×
n(Na+)=0.5mol×![]() =0.25mol;
=0.25mol;
(5)2L 1mol/LMgCl2中镁离子的物质的量为2L×1mol/L=2mol,Cl-的物质的量浓度为2mol/L;
(6)溶液中阴离子和阳离子的正负电荷守恒,即n(Na+)+2n( Mg2+)=n (Cl-)+2n(SO42-),所以0.2 mol+2×0.25 mol=0.4 mol+2n(SO42-),解出n(SO42-)=0.15mol,则SO42-的微粒个数为0.15NA。

 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案【题目】下列反应中,生成物所贮的化学能比反应物所贮化学能要多的是( )
A.CaO+H2O=Ca(OH)2
B.NaOH+HCl=NaCl+H2O
C.CH4+2O2 ![]() CO2+2H2O
CO2+2H2O
D.CO2+C ![]() 2CO
2CO
【题目】Li4Ti5O12和LiFePO4都是锂离子电池的电极材料,可利用钛铁矿(主要成分为FeTiO3,还含有少量MgO、SiO2等杂质)来制备,工艺流程如下:
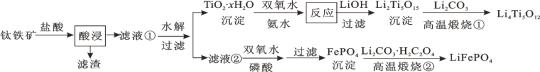
下列说法不正确的是
A.“酸浸”后,若钛主要以TiOCl42-形式存在,则相应反应的离子方程式可表示为:FeTiO3+4H++4Cl-=Fe2++TiOCl42-+2H2O
B.若Li2Ti5O15中Ti的化合价为+4,则其中过氧键的数目为3个
C.“高温煅烧②”中由FePO4制备LiFePO4的化学方程式可表示为:2FePO4+Li2CO3+H2C2O4![]() 2LiFeO4+H2O↑+3CO2↑
2LiFeO4+H2O↑+3CO2↑
D.TiO2·xH2O沉淀与双氧水、氨水反应40min所得实验结果如表所示:
温度/℃ | 30 | 35 | 40 | 45 | 50 |
TiO2·xH2O转化率/% | 92 | 95 | 97 | 93 | 88 |
可知,40℃前,未达到平衡状态,随着温度升高,转化率变大