题目内容
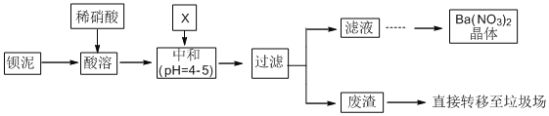
【题目】工业上利用硫铁矿烧渣(主要成分为Fe2O3、FeO、SiO2等)为原料制备高档颜料铁红(Fe2O3),具体生产流程如图:
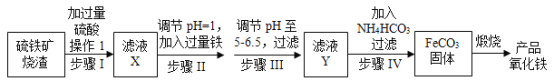
试回答下列问题:
(1)滤液X中含有的金属阳离子是___(填离子符号)。
(2)步骤Ⅱ中发生反应的离子方程式为_____。
(3)步骤Ⅲ中最好可选用___(填字母)调节溶液的pH。
A.稀硝酸 B.氨水 C.氢氧化钠溶液 D.高锰酸钾溶液
(4)步骤Ⅳ中,FeCO3沉淀完全后,溶液中含有少量Fe2+,检验Fe2+的方法是___。
(5)步骤Ⅳ的反应温度一般需控制在35℃以下,其目的是______。
(6)在空气中煅烧FeCO3生成产品氧化铁的化学方程式为_____。
【答案】Fe3+、Fe2+ Fe+2Fe3+=3Fe2+ B 取少量待测液于试管中,滴加少量K3Fe(CN)6溶液,若产生蓝色沉淀,则含Fe2+ 防止NH4HCO3受热分解 4FeCO3+O2![]() Fe2O3+4CO2
Fe2O3+4CO2
【解析】
硫铁矿烧渣酸浸时,二氧化硅不溶于酸,滤渣为二氧化硅;滤液为硫酸、硫酸铁、硫酸亚铁;加入适量铁粉,铁离子与铁粉反应生成亚铁离子;过滤除去稍过量的铁粉,加入碳酸氢铵产生碳酸亚铁沉淀,在空气中煅烧生成氧化铁;
(1)硫铁矿烧渣中含有氧化铁、氧化亚铁,酸浸时生成硫酸铁和硫酸亚铁,金属阳离子为Fe3+、Fe2+;
(2)步骤Ⅱ中铁粉与Fe3+反应生成Fe2+,离子方程式为Fe+2Fe3+=3Fe2+;
(3)步骤Ⅲ中含有的金属阳离子为Fe2+,调节pH的物质应不具备强氧化性,不引入新的杂质离子,答案为B;
(4)检验Fe2+常用的试剂为K3Fe(CN)6,方法为取少量待测液于试管中,滴加少量K3Fe(CN)6溶液,若产生蓝色沉淀,则含Fe2+;
(5)步骤Ⅳ加入的试剂为NH4HCO3,受热时容易分解,则控制的温度一般为35℃以下;
(6)在空气中煅烧FeCO3时,与空气中的氧气反应生成氧化铁和二氧化碳,方程式为4FeCO3+O2![]() Fe2O3+4CO2。
Fe2O3+4CO2。

 阅读快车系列答案
阅读快车系列答案