题目内容
7.下列反应中的氨的作用与4NH3+5O2→4NO+6H2O中氨的作用相同的是( )| A. | 2Na+2NH3=2NaNH2+H2↑ | B. | 3SiH4+4NH3=Si3N4+12H2 | ||
| C. | NH3+HCl=NH4Cl | D. | 2NH3+3CuO=3Cu+N2+3H2O |
分析 4NH3+5O2→4NO+6H2O反应中氨气中N元素的化合价升高,则氨气作还原剂,根据化合价的变化分析.
解答 解:A.2Na+2NH3→2NaNH2+H2↑反应中,NH3中N元素的化合价不变,故A错误;
B.3SiH4+4NH3=Si3N4+12H2反应中,H元素化合价由+1价变为0价、Si元素化合价由-4价变为+4价,所以是氧化还原反应,但氨气是氧化剂,故B错误;
C.HCl+NH3═NH4Cl反应中,没有元素化合价的变化,不是氧化还原反应,故C错误;
D.2NH3+3CuO=3Cu+N2+3H2O反应,气中N元素的化合价升高,则氨气作还原剂,故D正确.
故选D.
点评 本题考查了氨气的性质,侧重于氧化还原反应知识应用的考查,注意根据氨气中N元素的化合价变化分析,题目难度不大.

练习册系列答案
 能力评价系列答案
能力评价系列答案 唐印文化课时测评系列答案
唐印文化课时测评系列答案
相关题目
18.现有c(CH3COOH)=0.1mol/L的溶液,能使CH3COOH的电离平衡向右移动且能使c(CH3COO-)增大的是( )
| A. | 加大量水稀释 | B. | 降低温度 | C. | 加少量NaOH | D. | 加少量CH3COONa |
15.用NA表示阿伏加德罗常数,下列叙述正确的是( )
| A. | 物质的量浓度为0.5mol/L的MgCl2溶液中,含有Cl-个数为1NA | |
| B. | 常温常压下,1.7gH2O2中含有的电子数为0.8NA | |
| C. | 通常状况下,2.24LCO2和CO中所含分子数为0.1NA | |
| D. | 23gNO2和N2O4的混合气所含原子数为1.5NA |
19.按照物质的树状分类和交叉分类,HNO3应属于:①酸 ②氢化物 ③氧化物 ④含氧酸 ⑤难挥发性酸 ⑥强酸 ⑦化合物 ⑧混合物 ⑨弱电解质( )
| A. | ①④⑥⑦ | B. | ②③⑤⑧ | C. | ①②④⑨ | D. | ①⑥⑦⑨ |
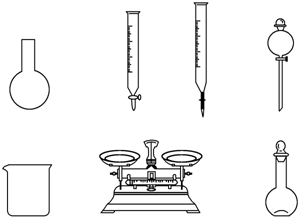 A.如图所示的仪器中,有四种是不需要的,还需一种玻璃仪器
A.如图所示的仪器中,有四种是不需要的,还需一种玻璃仪器