题目内容
12.请用氧化还原反应相关知识回答下列问题:某反应中反应物与生成物有:AsH3、H2SO4、KBrO3、K2SO4、H3AsO4、H2O和一种未知物质X.
①已知KBrO3在反应中得到电子,则该反应的还原剂是AsH3.
②KBrO3在反应中生成单质 X,则X的化学式为Br2.
③根据上述反应可推知ac.
a.氧化性:KBrO3>H3AsO4 b.氧化性:H3AsO4>KBrO3
c.还原性:AsH3>X d.还原性:X>AsH3
④在一定条件下,若发生了如下反应,请用双线桥表示该氧化还原反应:
5AsH3+4H2SO4+8KBrO3=4K2SO4+5H3AsO4+4H2O+4Br2.
分析 ①化合价升高元素所在的反应物是还原剂;
②根据溴元素化合价的降低情况来计算;
③氧化剂的氧化性最强,还原剂的还原性最强,氧化剂对应的产物叫还原产物;
④根据化学反应中化合价的升降情况标电子转移情况.
解答 解:①KBrO3在反应中得到电子,所以KBrO3是氧化剂,AsH3变成了H3AsO4,所以AsH3是还原剂,故答案为:AsH3;
②设X中溴元素的化合价为x,则0.2mol(5-x)=1mol,所以x=0,故X为Br2,故答案为:Br2;
③a、反应中KBrO3是氧化剂,H3AsO4是氧化产物,氧化性为KBrO3>H3AsO4,故a正确;
b、AsH3变成了H3AsO4,砷元素化合价升高,所以H3ASO4是氧化产物,故b错误;
c、AsH3是还原剂,Br2是还原产物,所以还原性AsH3>Br2,故c正确;
d、K2SO4和H2O中的元素化合价均未变化,既不是氧化产物也不是还原产物,故d错误.
故选ac;
④化合价升高的元素是砷元素,化合价从-3价升到+5价,化合价降低的元素是溴元素,化合价从+5价降到0价,化合价升高和降低数目得相等,所以转移40e-,
故答案为: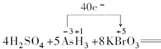 .
.
点评 本题考查学生氧化还原反应中的概念以及电子守恒定律的知识,综合性较强,难度较大.

练习册系列答案
 孟建平小学滚动测试系列答案
孟建平小学滚动测试系列答案
相关题目
2.下列对于“摩尔”的说法和理解正确的是( )
| A. | 摩尔是国际科学界建议采用的一种物理量 | |
| B. | 摩尔是物质的量的单位,简称摩,符号为mol | |
| C. | 国际上规定,0.012kg碳原子所含有的碳原子数目为1摩 | |
| D. | 摩尔可以把物质的宏观数量与微观粒子的数量联系起来 |
3.丁香油酚的结构如图示,从结构简式可推测化学性质叙述不正确的是( )


| A. | 可跟NaHCO3溶液反应放出CO2气体,又可使酸性KMnO4溶液褪色 | |
| B. | 可与三氯化铁溶液发生显色反应,又可与浓溴水发生取代反应 | |
| C. | 可与H2在一定条件下发生加成反应,又可与H2O在一定条件下发生加成反应 | |
| D. | 可与CH3COOH在稀硫酸作用下发生酯化反应,又可在稀硫酸作用下发生水解反应 |
20.0℃和101KPa条件下,13g某气体与8g CH4的分子数相同,则该气体在相应条件下的密度为( )
| A. | 0.58 g/L | B. | 0.29 g/L | C. | 1.16 g/L | D. | 0.714 g/L |
7.下列反应中的氨的作用与4NH3+5O2→4NO+6H2O中氨的作用相同的是( )
| A. | 2Na+2NH3=2NaNH2+H2↑ | B. | 3SiH4+4NH3=Si3N4+12H2 | ||
| C. | NH3+HCl=NH4Cl | D. | 2NH3+3CuO=3Cu+N2+3H2O |
17.已知下列热化学方程式:
①CH3COOH(l)+2O2(g)═2CO2(g)+2H2O(l)△H1=-870.3kJ/mol
②C(s)+O2(g)═CO2(g)△H2=-393.5kJ/mol
③H2(g)+$\frac{1}{2}$O2(g)═H2O(l)△H3=-285.8kJ/mol
则反应④2C(s)+2H2(g)+O2(g)═CH3COOH(l)的焓变为( )
①CH3COOH(l)+2O2(g)═2CO2(g)+2H2O(l)△H1=-870.3kJ/mol
②C(s)+O2(g)═CO2(g)△H2=-393.5kJ/mol
③H2(g)+$\frac{1}{2}$O2(g)═H2O(l)△H3=-285.8kJ/mol
则反应④2C(s)+2H2(g)+O2(g)═CH3COOH(l)的焓变为( )
| A. | 488.3 kJ/mol | B. | -224.15 kJ/mol | C. | -488.3 kJ/mol | D. | 244.15 kJ/mol |
4.下列液体中,不会出现丁达尔效应的分散系是( )
①鸡蛋清溶液 ②酒精 ③淀粉溶液 ④蔗糖溶液 ⑤FeCl3溶液 ⑥肥皂水.
①鸡蛋清溶液 ②酒精 ③淀粉溶液 ④蔗糖溶液 ⑤FeCl3溶液 ⑥肥皂水.
| A. | ②④⑤ | B. | ③④ | C. | ②④⑥ | D. | ④①③ |


 +2H2O.
+2H2O.