题目内容
【题目】碱式碳酸镁可用于牙膏、医药化妆品等工业,化学式为4MgCO3·Mg(OH)2·5H2O,某碱式碳酸镁中含有SiO2杂质,为测定其纯度。某兴趣小组设计了如下两个方案:
方案I:
取一定质量的样品,与硫酸充分反应,通过测定CO2的质量计算纯度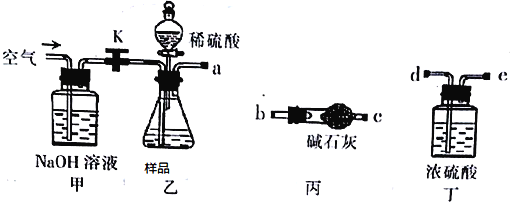
(1)乙中发生反应的方程式为______________________________ 。
(2)仪器接口的连接顺序为(装置可以重复使用) a__________,丁的作用是_________。
(3)关闭止水夹K,向样品中加入足量的稀硫酸,当样品充分反应完后,为了测定准确还应进行的操作是______________________________。
方案Ⅱ:
①称取碱式碳酸镁样品mg;②将样品充分高温灼烧,冷却后称量;③重复操作②,测得剩余固体质量为m1g(用托盘天平称量)。
(4)下列仪器中,该方案不会用到的是____________。
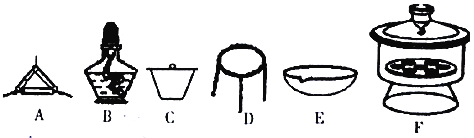
(5)有同学认为方案Ⅱ高温灼烧的过程中会发生MgCO3+SiO2![]() MgSiO3+CO2↑会导致测定结果有误,你认为这位同学的观点是否正确_____,(填“正确”或“错误”)请说明自己的理由:______________________。
MgSiO3+CO2↑会导致测定结果有误,你认为这位同学的观点是否正确_____,(填“正确”或“错误”)请说明自己的理由:______________________。
【答案】 4MgCO3·Mg(OH)2·5H2O+5H2SO4=5MgSO4+11H2O+4CO2↑ debcb 除去CO2中的水蒸气 打开止水夹K,缓慢通入空气 E 错误 该反应的发生不影响生成CO2和水蒸气的量
【解析】(1)碱式碳酸镁样品中含有的二氧化硅与硫酸不反应,而碱式碳酸镁4MgCO3·Mg(OH)2·5H2O,与硫酸反应生成硫酸镁、二氧化碳和水;反应的方程式为:4MgCO3·Mg(OH)2·5H2O+5H2SO4=5MgSO4+11H2O+4CO2↑;正确答案:4MgCO3·Mg(OH)2·5H2O+5H2SO4=5MgSO4+11H2O+4CO2↑。
(2)反应产生的二氧化碳气体中含有水蒸气,要先通过浓硫酸(长进短出)进行气体的干燥,然后纯净干燥二氧化碳被碱石灰吸收,最后称量出干燥管反应前后质量,根据质量差值即可计算出二氧化碳的纯度;外界空气中的水蒸气、二氧化碳进入丙装置,对实验有干扰,所以还要重复用丙装置,减少外界气体对实验带来的误差;仪器接口的连接顺序为:a debcb;丁装置的作用为除去CO2中的水蒸气;正确答案:debcb;除去CO2中的水蒸气。
(3)反应结束后整个装置内会存有少量的二氧化碳气体,这时,打开止水夹K,缓慢通入空气,使反应产生的二氧化碳气体全部被丙装置吸收,减少实验误差;正确答案:打开止水夹K,缓慢通入空气。
(4)给碱式碳酸镁样品加热,冷却、需要用到的仪器:坩埚、三脚架、酒精灯、泥三角、干燥器;用不到的仪器为蒸发皿;正确答案:E。
(5)方案Ⅱ操作过程中,最终测得剩余固体质量,而从样品中溢出的是二氧化碳和水蒸气,只要两种气体的总量不变,固体内部是否反应并不影响实验结果,所以该同学的观点不正确;答案:错误;该反应的发生不影响生成CO2和水蒸气的量。

 阅读快车系列答案
阅读快车系列答案【题目】下列实验中,对应的现象以及结论都正确且两者相符的是( )
选项 | A | B | C | D |
实 验 |
|
|
|
|
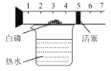
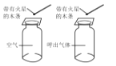
实 验 现 象 | 打开汽水瓶盖时,汽水 会自动喷出来 | 碘溶于水,几乎不溶于 汽油 | 白磷燃烧,产生大量白烟,活塞先向右再向左移,冷却至室温后,最终停在刻度“4”附近 | 空气中,带火星的木条复燃;呼出气体中,带火星的木条熄灭 |
实 验 结 论 | 说明气体在水中的溶解度随压强的增大而减小 | 说明物质的溶解性与溶剂的种类有关 | 氧气约占空气体积的五分之一 | 空气中的氧气比呼出气体中氧气多 |
A. A B. B C. C D. D
【题目】X、Y、Z、W是元素周期表前四周期中原子序数依次增大的常见元素,其相关信息如下表:
元素 | 相关信息 |
X | X的某种氢化物能使湿润的红色石蕊试纸变蓝 |
Y | Y的一种核素质量数为24.中子数为12 |
Z | Z的单质是良好的半导体材料,广泛应用于光电信息领域 |
W | W的最高价氧化物对应水化物是一种不溶于水的蓝色固体 |
回答下列问题:
(1)Y在元素周期表中的位置是________;X、Z的简单气态氢化物稳定性较弱的是____(填化学式)。
(2)X的一种氢化物X2H4的分子中极性键和非极性键数目比为_______;Y的氯化物电子式为________。
(3)W的氧化物(W2O)跟X的最高价氧化物对应的水化物反应生成XO的离子方程式为_______。