题目内容
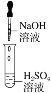
【题目】下图是实验室制氯气的装置。
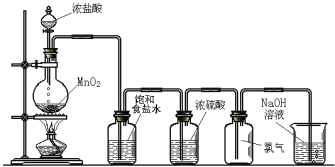
圆底烧瓶中发生反应的化学方程式为_____________________,生成1个Cl2分子转移电子数目为________个,饱和食盐水的作用是_____________________。
【答案】![]() 2 除去Cl2中混有的HCl气体
2 除去Cl2中混有的HCl气体
【解析】
实验室利用二氧化锰与浓盐酸在加热条件下制备氯气;根据电子守恒分析其电子转移数;制备的氯气中含有挥发的HCl。
二氧化锰与浓盐酸在加热条件下生成氯气、氯化锰和水,反应的化学方程式为:![]() ;氯元素化合价从-1价升高到0价,若生成1个Cl2分子,则转移电子数为2个;制备的氯气中含有少量挥发的HCl,氯气在饱和食盐水中溶解度不大,而氯化氢易溶于水,故选择排饱和食盐水的方法除去氯化氢,故答案为
;氯元素化合价从-1价升高到0价,若生成1个Cl2分子,则转移电子数为2个;制备的氯气中含有少量挥发的HCl,氯气在饱和食盐水中溶解度不大,而氯化氢易溶于水,故选择排饱和食盐水的方法除去氯化氢,故答案为![]() ;2;除去Cl2中混有的HCl气体。
;2;除去Cl2中混有的HCl气体。

【题目】依据事实,写出下列反应的热化学方程式。
(1)在25℃、101kPa下,1g甲醇(CH3OH)燃烧生成CO2和液态水时放热22.68kJ。则表示甲醇燃烧热的热化学方程式为___。
(2)25℃、101kPa若适量的N2和O2完全反应,每生成23gNO2需要吸收16.95kJ热量___。
(3)25℃、101kPa已知拆开1mol H-H键,1molN-H键,1molN≡N键分别需要的能量是436kJ、391kJ、946kJ,则N2与H2反应生成NH3的热化学方程式为___。
(4)甲醇既是重要的化工原料,又可作为燃料。利用合成气(主要成分为CO、CO2和H2)在催化剂作用下合成甲醇,发生的主要反应如下:
①CO(g)+2H2(g)![]() CH3OH(g) △H1
CH3OH(g) △H1
②CO2(g)+3H2(g)![]() CH3OH(g)+H2O(g) △H2
CH3OH(g)+H2O(g) △H2
③CO2(g)+H2(g)![]() CO(g)+H2O(g) △H3
CO(g)+H2O(g) △H3
回答下列问题:
已知反应①中相关的化学键键能数据如下:
化学键 | H—H | C—O | C | H—O | C—H |
E/(kJ·mol-1) | 436 | 343 | 1076 | 465 | 413 |
由此计算△H1=___kJ·mol-1,已知△H2=-58kJ·mol-1,则△H3=___kJ·mol-1。
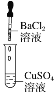
【题目】某同学在实验室中进行如下实验:
编号 | Ⅰ | Ⅱ | Ⅲ |
实验 |
|
|
|
现象 | 没有明显变化,溶液仍为无色 | 有沉淀生成,溶液为蓝绿色 | 有无色气泡产生 |
以下结论不正确的是( )
A.Ⅰ中无明显变化,说明两溶液不反应
B.Ⅱ中的白色沉淀为BaSO4
C.Ⅲ中发生的反应是离子反应
D.Ⅲ中发生反应的离子方程式为2H++Zn=Zn2++H2↑