题目内容
16.下列物质的水溶液中,呈酸性的是( )| A. | CO2 | B. | NaOH | C. | NaHCO3 | D. | K2SO4 |
分析 物质的水溶液呈酸性,说明该物质为酸或强酸弱碱盐,酸电离出氢离子或盐中弱离子水解导致溶液呈酸性,据此分析.
解答 解:A、二氧化碳为酸性气体,溶于水后生成碳酸,故水溶液显酸性,故A正确;
B、NaOH为强碱,溶于水后显碱性,故B错误;
C、碳酸氢钠中碳酸氢根离子水解程度大于电离程度,所以碳酸氢钠溶液呈碱性,故C错误;
D、硫酸钾为强酸强碱盐,在水溶液中不水解,显中性,故D错误.
故选A.
点评 本题考查了溶液酸碱性的判断,根据物质的性质及盐类水解特点来分析解答,溶液呈酸性,该溶液中的溶质可能是酸或盐,很多同学往往漏掉盐而导致错误,为易错点.

练习册系列答案
 培优口算题卡系列答案
培优口算题卡系列答案 开心口算题卡系列答案
开心口算题卡系列答案 口算题卡河北少年儿童出版社系列答案
口算题卡河北少年儿童出版社系列答案
相关题目
6.下列关于氯水的说法正确的是( )
| A. | 向氯水中通入二氧化硫,氯水的漂白性增强 | |
| B. | 氯水中加入NaCl固体,对溶液的pH无影响 | |
| C. | 常温下,pH=2的氯水中:c (Cl-)+c ( ClO-)+c (OH -)=0.01mol•L-1 | |
| D. | 向氯水中滴加少量NaHCO3溶液的离子反应方程式为:Cl2+2HCO3-═2CO2↑+Cl -+ClO -+H2O |
4.下列事实不能证明HNO2是弱电解质的是( )
| A. | 常温下0.001 mol/L和0.10 mol/L 的HNO2溶液,分别用pH计测它们的pH,两者的pH相差小于2个单位 | |
| B. | 常温下90mL0.1 mol•L-1 HNO2溶液导电性比10mL0.1 mol•L-1 HCl溶液弱 | |
| C. | 10mL0.1 mol•L-1的HNO2与0.1 mol•L-1的NaOH恰好完全反应时,消耗10mLNaOH | |
| D. | 浓度相同的 HNO2溶液与NaNO2溶液中,后者NO2-浓度大 |
1.现有500ml 1mol/L KCl 溶液,下列哪项的Cl-浓度与之相等( )
| A. | 100ml 5mol/L KCl | B. | 250ml 5mol/L MgCl2 | ||
| C. | 100ml 1mol/L CaCl2 | D. | 250ml 1mol/L NaCl |
5.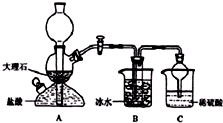 在实验室中,可利用碳酸氢钠、氯化钠、氯化铵等物质溶解度的差异,通过饱和食盐水、氨和二氧化碳反应,获得碳酸氢钠晶体,反应原理可用如下化学方程式表示:NH3+CO2+NaCl+H2O═NH4Cl+NaHCO3↓,依据此原理,欲制得碳酸氢钠晶体,某校学生设计了如图实验装置,其中B装置中的试管内是溶有氨和氯化钠的溶液,且二者均已达到饱和:
在实验室中,可利用碳酸氢钠、氯化钠、氯化铵等物质溶解度的差异,通过饱和食盐水、氨和二氧化碳反应,获得碳酸氢钠晶体,反应原理可用如下化学方程式表示:NH3+CO2+NaCl+H2O═NH4Cl+NaHCO3↓,依据此原理,欲制得碳酸氢钠晶体,某校学生设计了如图实验装置,其中B装置中的试管内是溶有氨和氯化钠的溶液,且二者均已达到饱和:
(1)A装置中所发生反应的离子方程式为:CaCO3+2H+═Ca2++CO2↑+H2O.C装置中稀硫酸的作用为:吸收从B装置中的试管内逸出的氨气,减少对环境的污染.
(2)下表中所列出的是相关物质在不同温度下的溶解度数据(g/100g水)
参照表中数据,请分析B装置中使用冰水是因为温度越低,碳酸氢钠的溶解度越小,便于析出.
(3)该校学生在检查完此套装置气密性后进行实验,结果没有得到碳酸氢钠晶体,指导教师指出应在A装置B之间(填写字母)连接一个盛有饱和NaHCO3溶液 的洗气装置,其作用是除去CO2中混有的HCl气体.
(4)利用改进后的装置进行实验,在B中的试管内析出了晶体,经必要的操作后得到了一种纯净的晶体.请通过简单实验判断该晶体是碳酸氢钠晶体而不是碳酸氢铵晶体,简述操作方法、实验现象及结:取少量晶体置于试管中,在酒精灯上加热使其充分反应后,还有白色固体剩余,则
晶体不是NH4HCO3.
(5)若该校学生进行实验时,所用饱和食盐水中含NaCl的质量为5.85g,实验后得到干燥的NaHCO3晶体的质量为5.88g,则NaHCO3的产率为70%.
 在实验室中,可利用碳酸氢钠、氯化钠、氯化铵等物质溶解度的差异,通过饱和食盐水、氨和二氧化碳反应,获得碳酸氢钠晶体,反应原理可用如下化学方程式表示:NH3+CO2+NaCl+H2O═NH4Cl+NaHCO3↓,依据此原理,欲制得碳酸氢钠晶体,某校学生设计了如图实验装置,其中B装置中的试管内是溶有氨和氯化钠的溶液,且二者均已达到饱和:
在实验室中,可利用碳酸氢钠、氯化钠、氯化铵等物质溶解度的差异,通过饱和食盐水、氨和二氧化碳反应,获得碳酸氢钠晶体,反应原理可用如下化学方程式表示:NH3+CO2+NaCl+H2O═NH4Cl+NaHCO3↓,依据此原理,欲制得碳酸氢钠晶体,某校学生设计了如图实验装置,其中B装置中的试管内是溶有氨和氯化钠的溶液,且二者均已达到饱和:(1)A装置中所发生反应的离子方程式为:CaCO3+2H+═Ca2++CO2↑+H2O.C装置中稀硫酸的作用为:吸收从B装置中的试管内逸出的氨气,减少对环境的污染.
(2)下表中所列出的是相关物质在不同温度下的溶解度数据(g/100g水)
| 0℃ | 10℃ | 20℃ | 30℃ | 40℃ | 50℃ | |
| NaCl | 35.7 | 35.8 | 36.0 | 36.3 | 36.6 | 37.0 |
| NaHCO3 | 6.9 | 8.1 | 9.6 | 11.1 | 12.7 | 14.5 |
| NH4Cl | 29.4 | 33.3 | 37.2 | 41.4 | 45.8 | 50.4 |
(3)该校学生在检查完此套装置气密性后进行实验,结果没有得到碳酸氢钠晶体,指导教师指出应在A装置B之间(填写字母)连接一个盛有饱和NaHCO3溶液 的洗气装置,其作用是除去CO2中混有的HCl气体.
(4)利用改进后的装置进行实验,在B中的试管内析出了晶体,经必要的操作后得到了一种纯净的晶体.请通过简单实验判断该晶体是碳酸氢钠晶体而不是碳酸氢铵晶体,简述操作方法、实验现象及结:取少量晶体置于试管中,在酒精灯上加热使其充分反应后,还有白色固体剩余,则
晶体不是NH4HCO3.
(5)若该校学生进行实验时,所用饱和食盐水中含NaCl的质量为5.85g,实验后得到干燥的NaHCO3晶体的质量为5.88g,则NaHCO3的产率为70%.
6. 在10L恒容密闭容器中充入X(g)和Y(g),发生反应X(g)+Y(g)?M(g)+N(g)所得实验数据如表:
在10L恒容密闭容器中充入X(g)和Y(g),发生反应X(g)+Y(g)?M(g)+N(g)所得实验数据如表:
回答下列问题:
(1)实验①中,若5min时测得,n(M)=0.050mo1,则0至5min时间内,用N表示的平均反应速率为1.0×10-3mol/(L•min).
(2)实验③平衡常数为1.0,该正反应为放热反应(填“吸热”或“放热”)
(3)能说明上述反应一定达到平衡的条件是C.
A.c(Y)=c(N) B.平均分子量不再变化
C.v正(X)=v逆(M) D.温度和压强一定时,混合气体的密度不再变化
(4)实验③中,达到平衡时,X的转化率为60%多余.
(5)实验③、④中,达到平衡时,a与b的关系为A(填选项),请解释原因若温度不变,则b=$\frac{1}{2}$a,该反应为放热反应,温度升高,平衡向逆反应方向移动,故b<$\frac{1}{2}$a,即a>2b.
A.a>2b B.a=2b C.b<a<2b D.a<b
(6)如图是实验①中c(M)随时间变化的曲线图,请在图中画出实验②中c(M)随时间变化的曲线图.
 在10L恒容密闭容器中充入X(g)和Y(g),发生反应X(g)+Y(g)?M(g)+N(g)所得实验数据如表:
在10L恒容密闭容器中充入X(g)和Y(g),发生反应X(g)+Y(g)?M(g)+N(g)所得实验数据如表:| 实验编号 | 温度/℃ | 起始时物质的量/mol | 平衡时物质的量/mol | |
| n(X) | n(Y) | n(M) | ||
| ① | 700 | 0.40 | 0.10 | 0.090 |
| ② | 800 | 0.10 | 0.40 | 0.080 |
| ③ | 800 | 0.20 | 0.30 | a |
| ④ | 900 | 0.10 | 0.15 | b |
(1)实验①中,若5min时测得,n(M)=0.050mo1,则0至5min时间内,用N表示的平均反应速率为1.0×10-3mol/(L•min).
(2)实验③平衡常数为1.0,该正反应为放热反应(填“吸热”或“放热”)
(3)能说明上述反应一定达到平衡的条件是C.
A.c(Y)=c(N) B.平均分子量不再变化
C.v正(X)=v逆(M) D.温度和压强一定时,混合气体的密度不再变化
(4)实验③中,达到平衡时,X的转化率为60%多余.
(5)实验③、④中,达到平衡时,a与b的关系为A(填选项),请解释原因若温度不变,则b=$\frac{1}{2}$a,该反应为放热反应,温度升高,平衡向逆反应方向移动,故b<$\frac{1}{2}$a,即a>2b.
A.a>2b B.a=2b C.b<a<2b D.a<b
(6)如图是实验①中c(M)随时间变化的曲线图,请在图中画出实验②中c(M)随时间变化的曲线图.
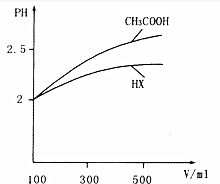 (1)常温下,0.1mol•L-1的CH3COOH溶液加水稀释过程中,下列表达式的数据变大的是BD(填序号)
(1)常温下,0.1mol•L-1的CH3COOH溶液加水稀释过程中,下列表达式的数据变大的是BD(填序号) 恒温恒容时,NO2和N2O4之间发生反应N2O4(g)?2NO2(g),如图所示.
恒温恒容时,NO2和N2O4之间发生反应N2O4(g)?2NO2(g),如图所示.