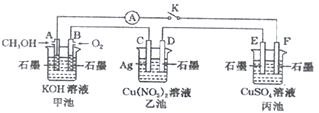
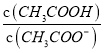��Ŀ����
����Ŀ����1����2L�����ܱ�������ͨ��1molN2(g)��3molH2(g),������Ӧ��
3H2(g)+N2(g)![]() 2NH3(g)��H<0,���ѹǿһʱ��ͼ����ͼ�ף����p2=0.6p1����ʱ�¶�����ʼ�¶���ͬ���ڴﵽƽ��ǰijһʱ��(t1)�����ı�һ���������õ�����ͼ��
2NH3(g)��H<0,���ѹǿһʱ��ͼ����ͼ�ף����p2=0.6p1����ʱ�¶�����ʼ�¶���ͬ���ڴﵽƽ��ǰijһʱ��(t1)�����ı�һ���������õ�����ͼ��
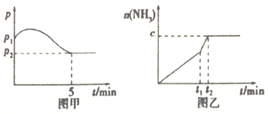
����ͼ��c=1.6mol,��ı��������__________(����ĸ����ͬ);
A������ B������ C����ѹ D����ѹ E���Ӵ���
����ͼ��c<1.6mol,��ı��������__________(����ĸ);��ʱ�÷�Ӧ��ƽ�ⳣ��__________(���������С���������䡱)��
��2����ͼ�ף�ƽ��ʱ������ת����Ϊ____________��
���Ƶ�CuCl2��2H2O�����г�����Fe3+��Fe2+���ʣ�Ϊ�Ƶô������Ȼ�ͭ���壬���Ƚ����Ƴ�ˮ��Һ���ٰ���ͼ��ʾ�IJ�����������ᴿ��
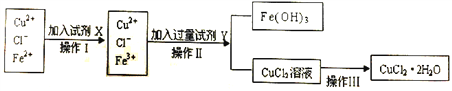
��1��������ʱ�����ȼ�����ʵ�����������Fe2+����ΪFe3+,���п�ѡ�õ���������__________��
A��KMnO4 B��H2O2 C��Cl2 D��HNO3
��2�������������Һ��pH��Y�Լ���ѡ�������е�__________��
A��NaOH(s) B����ˮ C��CuO(s) D��Cu(OH)2(s)
��3����֪�ܶȻ��������±���
���� | Cu(OH) | Fe(OH)2 | Fe(OH)3 |
Ksp | 2.2��10-20 | 8.0��10-16 | 4.0��10-38 |
����Һ��pH����pH=4ʱ��ʹFe3+��ȫת��ΪFe(OH)3��������ȥ����ʱc(Fe3+)=__________��
��4������CuCl2��Һ���ɺ������գ��õ��Ĺ�����__________(�ѧʽ);���������CuCl2��2H2O����õ�������ˮCuCl2�ĺ���������_____________________________________��
���𰸡� E A ��С 80% BC CD 4.0��10-8molL-1 CuO �ڸ����HCl����������
����������1���ٴ�ͼ����Կ�����c=1.6mol����Ӧ��ƽ��״̬��ֻ��ʹ�ô�����ƽ���ƶ���Ӱ������ȷѡ�E��
�ڸ÷�Ӧ����ӦΪ���ȷ�Ӧ�������¶���ƽ��������c<1.6mol����ȷѡ�A������ƽ�����ƣ��¶����ߣ���Ӧ��Ũ������������Ũ�ȼ��٣��÷�Ӧ��ƽ�ⳣ�����٣���ȷ�𰸣����٣�
��2����÷�Ӧ�����ĵ���Ϊxmol, ��Ӧǰ�����������֮�ȵ���ѹǿ֮�ȣ�
3H2(g) + N2(g)![]() 2NH3(g)
2NH3(g)
��ʼ�� 3 1 0
�仯�� 3x x 2x
ƽ���� 3-3x 1- x 2x
p2/p1=(3-3x+1-x+2x)/ (3 +1)=0.6��x=0.8��ƽ��ʱ������ת����Ϊ0.8��1��100%=80%����ȷ��80%��
��1��A��KMnO4��Fe2+����ΪFe3+, ��������������������K+ ��Mn2+����������A������B��H2O2 �Ļ�ԭ������ˮ����һ����ɫ��������B��ȷ��C��Cl2�ܰ�Fe2+����ΪFe3+,
������ΪCl-��û�������������ӣ�C��ȷ��D��HNO3�Ļ�ԭ�����ǵ������������Ի�����Σ����D��������ȷ��ѡ��BC��
��2��������Һ��pHʱ��Ҫ�������к����ͬʱ�����������������ӽ�����Һ�У� ʣ������ʻ����ڳ�ȥ��CuO ��Cu(OH)2���ֹ��嶼������ˮ�����ܹ����������ܹ��ﵽ���ص�Ŀ������ȷѡ����C D��
��3������Ksp=c(Fe3+)c3 (OH-)��pH����pH=4��c(H+)=10-4, c(OH-)=10-10�����빫ʽ��
4.0��10-38= c(Fe3+)��c3 (OH-)= c(Fe3+)��10-30��c(Fe3+)=4.0��10-8molL-1����ȷ��4.0��10-8molL-1��
��4���Ȼ�ͭ��Һˮ�⣺CuCl2+2H2O![]() Cu(OH)2+2HCl����Һ���ɺ��Ȼ���ӷ���������������ͭ�õ��Ĺ���������ͭ�������Ȼ�ͭ��Һ����ˮ�⣬ֻ���ڲ���ͨ���Ȼ�������������£������Ȼ�ͭ��ˮ�⣬�����ڼ������ɵ�����µõ���������ˮCuCl2 ������
Cu(OH)2+2HCl����Һ���ɺ��Ȼ���ӷ���������������ͭ�õ��Ĺ���������ͭ�������Ȼ�ͭ��Һ����ˮ�⣬ֻ���ڲ���ͨ���Ȼ�������������£������Ȼ�ͭ��ˮ�⣬�����ڼ������ɵ�����µõ���������ˮCuCl2 ������
��ȷ�𰸣�CuO ���ڸ����HCl������������

 ��У����ϵ�д�
��У����ϵ�д�