��Ŀ����
4��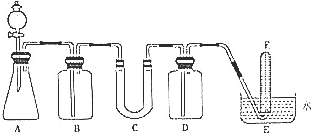 �ں�����ߺ�DZˮͧ�п��ù���������Ϊ����������ѡ���ʵ��Ļ�ѧ�Լ���ʵ����Ʒ����ͼ�е�ʵ��װ�ý���ʵ�飬֤���������ƿ�����������
�ں�����ߺ�DZˮͧ�п��ù���������Ϊ����������ѡ���ʵ��Ļ�ѧ�Լ���ʵ����Ʒ����ͼ�е�ʵ��װ�ý���ʵ�飬֤���������ƿ�������������1����д���пո�
| ���� | �����Լ� | ������Լ���Ŀ�� |
| B | ����NaHCO3��Һ | ��ȥCO2�����л����HCl |
| C | ʯ������������� | ��CO2��ˮ����Ӧ������O2 |
| D | NaOH | ����δ��Ӧ��CO2���� |
A.5.8 B.11.6 C.23.2 D.46.4
��3���Թ�F�ռ����������һ��ʵ������ǰ�F�еĵ����Ƴ�ˮ�棬�رշ�Һ©����������Ĵָ��ס�Թܿڣ�ȡ���Թܣ������Ѵ����ǵ�ľ�������Թܿ��ڣ�ľ����ȼ��֤���Թ����ռ�������������
��4��ij�˰����з��̲ⶨ��Ʒ��Na2O2�ĺ�������ȡһ������Ʒ����������ˮ��������Ӧ��Na2O2+2H2O=2NaOH+H2O2��2H2O2$\frac{\underline{\;NaOH\;}}{\;}$2H2O+O2������������O2����������Ʒ��Na2O2�Ĵ��ȣ�����ϸʵ�����Σ��õ���Na2O2���������Ե���ʵ�ʺ�����������ΪB��
A����������
B��H2O2�ֽⲻ��ȫ
C��Na2O2ת��ΪH2O2��NaOH�ķ�Ӧ����ȫ
D��װ��©����
���� ��1����ʵ��װ�ÿ�֪����ʵ��������CaCO3�����ᷴӦ����CO2����������ͨ������NaHCO3��Һ���Գ�ȥCO2�����л����HCl��Ȼ�����������CO2��ˮ����Ӧ������O2������ˮ���ռ�O2�����ȡ���Թܣ������Ѵ����ǵ�ľ�������Թܿ��ڣ�ľ����ȼ��֤���Թ����ռ���������������
��2���������Ĺ���Na2O2��ͨ��11.6gCO2��H2O��������Ӧ����ʽΪ��2Na2O2+2CO2=Na2CO3+O2��2Na2O2+2H2O=4NaOH+O2��������ֻ������3.6g������Ϊ����O2�����������غ㶨�ɿ�֪m��O2��=11.6g-3.6g=8g������n=$\frac{m}{M}$�����������������ʵ��������ݷ���ʽ��֪n��������壩=2n��O2������������ԭ��������ƽ����Է���������
��3��������������֤����������
��4�������������Σ��������dz�������װ��©����ԭ��Ȼ���Ϸ�Ӧ����ʽ��������Na2O2���������Ե���ʵ�ʺ�����ԭ��
��� �⣺��1����������ͨ������NaHCO3��Һ���Գ�ȥCO2�����л����HCl��Ȼ�����������CO2��ˮ����Ӧ������O2���������ɵ������л��ж�����̼���壬Ӧ��NaOH��Һϴ��������δ��Ӧ��CO2���壬����ˮ���ռ�O2��
�ʴ�Ϊ��
| ���� | �����Լ� | ������Լ���Ŀ�� |
| B | ��ȥCO2�����л����HCl | |
| C | �������� | ��CO2��ˮ����Ӧ������O2 |
| D | NaOH��Һ | ����δ��Ӧ��CO2���� |
���ݷ���ʽ2Na2O2+2CO2=Na2CO3+O2��2Na2O2+2H2O=4NaOH+O2����֪n��������壩=2n��O2��=2��0.25mol=0.5mol��
����ԭ��������ƽ��Ħ������Ϊ��$\frac{11.6g}{0.5mol}$=23.2g/mol���ʻ�������ƽ����Է�������Ϊ23.2��
�ʴ�Ϊ��23.2��
��3����ʵ���Ŀ��Ϊ֤���������ƿ������������ռ������Ҫ��֤�Ƿ�Ϊ������Ϊ��ֹ������Ӧ�Ȱ�F�еĵ����Ƴ�ˮ�棬Ȼ��رշ�Һ©���������ô����ǵ�ľ�������Թܿ��ڣ�ľ����ȼ��֤���Թ����ռ���������������
�ʴ�Ϊ����F�еĵ����Ƴ�ˮ�棬�رշ�Һ©����������Ĵָ��ס�Թܿڣ�ȡ���Թܣ������Ѵ����ǵ�ľ�������Թܿ��ڣ�ľ����ȼ��֤���Թ����ռ���������������
��4��A�����ڷ��������Σ���������Ϊ����������Na2O2���������Ե���ʵ�ʺ�������A����
B��H2O2�ֽⲻ��ȫ���ڷ�Ӧ�����Һ�д��ڲ���˫��ˮ���ӣ��ᵼ�����ɵ���������ƫС����õ���Na2O2���������Ե���ʵ�ʺ�������B��ȷ��
C��Na2O2ת��ΪH2O2��NaOH�ķ�Ӧ����ȫ��Ӧ�������ܳ��ָ÷�Ӧ����ȫ����C����
D�����������Σ�������Ϊװ��©������Na2O2���������Ե���ʵ�ʺ�������D����
��ѡB��
���� ���⿼�����������鷽������������ۣ���Ŀ�Ѷ��еȣ���ȷ����������ˮ��Ӧ��ԭ��Ϊ���ؼ���ע�������������鷽�������������ԭ������������ѧ���ķ�����������ѧʵ��������

 ������ҵ��ͬ����ϰ��ϵ�д�
������ҵ��ͬ����ϰ��ϵ�д�| A�� | 1 mol OH-�к���10NA������ | |
| B�� | 46g��NO2�������NA��NO2���� | |
| C�� | 1 L 1 mol/L��AlCl3��Һ�к���NA��Al3+ | |
| D�� | ���³�ѹ��11.2 L�ļ������庬�еķ�����Ϊ0.5NA |
�ٵ�3���ڵ�һ��������С��Ԫ�� ����Χ���ӹ���Ϊ2s22p6��ԭ�� ��2p���Ϊ������Ԫ�� �ܵ縺������Ԫ�أ�
| A�� | �٢� | B�� | �ۢ� | C�� | �ڢ� | D�� | �٢� |
| A�� | 10mL | B�� | 20mL | C�� | 50mL | D�� | 100mL |
| ���� | CH3COOH | H2CO3 | HNO2 |
| ���볣����25�棩 | K=1.8��10-5 | K1=4.3��10-7 K2=5.6��10-11 | K=5.0��10-4 |
��1�����¶��£���0.1mol��L-1CH3COOH ��Һ�м�������CH3COONa ����ʱ������˵����ȷ����ad������ţ���
a����Һ��pH���� b�� CH3COOH�ĵ���̶�����
c����Һ�ĵ����������� d����Һ��c��OH- ��•c��H+ ������
��2��25��ʱ��0.10mol��L-1 Na2CO3 ��Һ��pH=11������Һ����ˮ�������c��OH- ����10-3mol��L-1
��3�������£���20mL 0.10mol��L-1 CH3COOH��Һ��20mL 0.10mol��L-1 HNO2 ��Һ�ֱ���20mL 0.10mol��L-1 NaHCO3 ��Һ��ϣ���Ϻ���Һ����仯���Բ��ƣ���
�ٷ�Ӧ��ʼʱ��v��CH3COOH ���� v��HNO2�������������������������ԭ���Ǿ������ƽ�ⳣ����֪��HNO2�����Աȴ���ǿ����������Ա�̼��ǿ����ͬ���ʵ���Ũ�ȵĴ����HNO2��ȣ�HNO2��Һ��������Ũ�ȴ�������̼��������Һ��Ӧ���ʿ죮
�ڳ�ַ�Ӧ������Һ��c��CH3COO-����c��NO2-�������������������=������
��4��25��ʱ����CH3COOH��Һ�м���һ������NaHCO3�����û��Һ��pH=6������Һ��$\frac{c��C{H}_{3}CO{O}^{-}��}{c��C{H}_{3}COOH��}$=18��
| A�� | 1��1 | B�� | 2��1 | C�� | 1��2 | D�� | ����� |
| A�� | Al3++2NH4++5OH-=Al��OH��3��+2NH3•H2O | |
| B�� | 2Al3++NH4++7OH-=2Al��OH��3+NH3•H2O | |
| C�� | Al3++4NH4++8OH-=4NH3•H2O+AlO2-+2H2O | |
| D�� | Al3++2NH4++6OH-=AlO2-+2NH3•H2O+2H2O |
| A�� | ��ⷨ����ʱһ���������ڵ����������е�⣬��Ҳ������Ӧ���Σ�������̬�������� | |
| B�� | ��ⷨ������ʱ���������������ᴿ�����ᴿ������Ӧ�������������������������� | |
| C�� | ���ȼҵ�У������е�������������Na0H��H2 | |
| D�� | �ȼҵ�ͽ����Ƶ������ж��õ���NaCl���ڵ��ʱ���ǵ���������Cl-ʧ���� |
| A�� | 30 g•mol-1��46 g•mol-1 | B�� | 44 g•mol-1��80 g•mol-1 | ||
| C�� | 28 g•mol-1 | D�� | 46 g•mol-1 |