题目内容
7.下列微粒中原子最外层电子数均为8的是( )| A. | PCl5 | B. | NO2 | C. | NF3 | D. | H2O |
分析 根据判断的技巧:原子的最外层电子数+化合价绝对值=8,则该原子的最外层为8电子结构.
解答 解:A、磷原子的最外层电子数+化合价绝对值为10,不是8电子结构,故A错误;
B、氮原子的最外层电子数+化合价绝对值为9,不是8电子结构构,故B错误;
C、氮原子和氟原子的最外层电子数+化合价绝对值为8,则原子的最外层均为8电子结构,故C正确;
D、氢原子最外层为2电子结构,而不是8电子结构,故D错误.
故选C.
点评 本题是对学生原子结构知识的考查,注意规律性的知识在解决选择题中的作用和地位.

练习册系列答案
 口算心算速算应用题系列答案
口算心算速算应用题系列答案 同步拓展阅读系列答案
同步拓展阅读系列答案
相关题目
17.已知下列三个反应:2Fe3++2I-═2Fe2++I2;2Fe2++Cl2═2Fe3++2Cl-;2MnO4-+10Cl-+16H+═2Mn2++5Cl2↑+8H2O,某溶液中有Fe2+、Cl-和I-,要氧化除去I-而又不影响Fe2+和Cl-,可加入的试剂是( )
| A. | Cl2 | B. | KMnO4 | C. | 浓HCl | D. | FeCl3 |
18.(1)下表是元素周期表的一部分,针对表中的①~⑨种元素,填写下列空白:
在最高价氧化物的水化物中,酸性最强的化合物的分子式是HClO4,碱性最强的化合物的电子式是: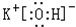 .
.
(2)在盛有500mL 0.1mol/LCuSO4溶液的大烧杯中.用锌、铜作电极,用导线连接形成原电池,写出电极反应式:负极Zn-2e-=Zn2+; 正极Cu2++2e-=Cu.
(3)过量的锌粉与一定量的稀盐酸反应,为了减慢反应速率,但是又不影响生成的氢气总量,可以采取的措施是B
A.升高温度 B.加入适量的水 C.加入少量CuSO4溶液 D.加入浓度较大的盐酸.
| 主族 周期 | ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | 0族 |
| 2 | ① | ② | ③ | |||||
| 3 | ④ | ⑤ | ⑥ | ⑦ | ⑧ | |||
| 4 | ⑨ |
 .
.(2)在盛有500mL 0.1mol/LCuSO4溶液的大烧杯中.用锌、铜作电极,用导线连接形成原电池,写出电极反应式:负极Zn-2e-=Zn2+; 正极Cu2++2e-=Cu.
(3)过量的锌粉与一定量的稀盐酸反应,为了减慢反应速率,但是又不影响生成的氢气总量,可以采取的措施是B
A.升高温度 B.加入适量的水 C.加入少量CuSO4溶液 D.加入浓度较大的盐酸.
2.某化学兴趣小组要完成中和热的测定.
(1)实验桌上备有烧杯(大、小两个烧杯)、泡沫塑料、泡沫塑料板、胶头滴管、环形玻璃搅拌棒、0.5mol•L-1 盐酸、0.55mol•L-1NaOH溶液,
尚缺少的实验玻璃用品是量筒、温度计.
(2)实验中能否用环形铜丝搅拌棒代替环形玻璃搅拌棒?否(填“能”或“否”),其原因是金属易导热,热量散失导致误差大.
(3)他们记录的实验数据如下:
已知:Q=Cm(t2-t1),反应后溶液的比热容C为4.18KJ•℃-1•Kg-1,各物质的密度均为1g•cm-3.计算完成上表.
(4)实验中NaOH的浓度比HCl的大,其原因是确保盐酸完全反应,使反应更充分
(5)若用KOH代替NaOH,对测定结果无(填“有”或“无”)影响;若用醋酸代替HCl做实验,则测定结果偏低(填“偏高”“偏低”或“无影响”).
(1)实验桌上备有烧杯(大、小两个烧杯)、泡沫塑料、泡沫塑料板、胶头滴管、环形玻璃搅拌棒、0.5mol•L-1 盐酸、0.55mol•L-1NaOH溶液,
尚缺少的实验玻璃用品是量筒、温度计.
(2)实验中能否用环形铜丝搅拌棒代替环形玻璃搅拌棒?否(填“能”或“否”),其原因是金属易导热,热量散失导致误差大.
(3)他们记录的实验数据如下:
| 实 验 用 品 | 溶 液 温 度 | 中和热 △H | |||
| t1 | t2 | ||||
| ① | 50mL0.55mol.L-1NaOH | 50mL.0.5mol.L-1HCl | 20℃ | 23.3℃ | |
| ② | 50mL0.55mol.L-1NaOH | 50mL.0.5mol.L-1HCl | 20℃ | 23.5℃ | |
(4)实验中NaOH的浓度比HCl的大,其原因是确保盐酸完全反应,使反应更充分
(5)若用KOH代替NaOH,对测定结果无(填“有”或“无”)影响;若用醋酸代替HCl做实验,则测定结果偏低(填“偏高”“偏低”或“无影响”).
12.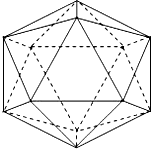 单质硼有无定形和晶体两种,参考下表数据
单质硼有无定形和晶体两种,参考下表数据
(1)晶体硼的晶体类型属于原子晶体,理由是熔、沸点很高、硬度很大.
(2)已知晶体硼结构单元是由硼原子组成的正二十面体,其中有20个等边三角形的面和一定数目的顶点,每个项点上各有1个B原子.通过视察图形及推算,此晶体体结构单元由12个硼原子构成.其中B-B键的键角为60°.共含有30个B-B.
 单质硼有无定形和晶体两种,参考下表数据
单质硼有无定形和晶体两种,参考下表数据| 金刚石 | 晶体硅 | 晶体硼 | |
| 熔点 | 3823 | 1683 | 2573 |
| 沸点 | 5100 | 2628 | 2823 |
| 硬度 | 10 | 7.0 | 9.5 |
(2)已知晶体硼结构单元是由硼原子组成的正二十面体,其中有20个等边三角形的面和一定数目的顶点,每个项点上各有1个B原子.通过视察图形及推算,此晶体体结构单元由12个硼原子构成.其中B-B键的键角为60°.共含有30个B-B.
16.日前中国量子物质科学协同创新中心的江颖课题组和王恩哥课题组合作,在水科学领域取得重大突破,在国际上首次实现了水分子的亚分子级分辨成像,使得解析水的氢键网络构型成为可能.(图a是实验器件示意图,图b是拍摄到的图片的一部分,图c是图b所对应的结构示意图)下列有关说法不正确的是( )
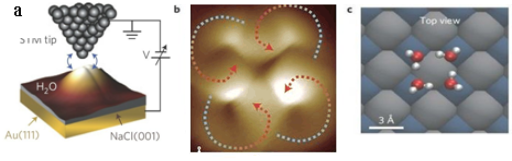

| A. | 图a所示实验器件中,用氯化钠作为绝缘薄膜层,是因为氯化钠晶体不导电 | |
| B. | 图b是表示一个H2O分子内部的氢键和氢氧共价键结构特征示意图 | |
| C. | 水分子间形成氢键使水的熔点和沸点升高 | |
| D. | H2O分子的稳定性很强,是因为分子内氢氧共价键强 |
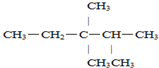 2,3,3-三甲基戊烷;
2,3,3-三甲基戊烷;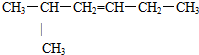 2-甲基-3-己烯;
2-甲基-3-己烯;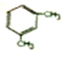 1,3-二甲基苯.(用系统命名法命名)
1,3-二甲基苯.(用系统命名法命名)