题目内容
16.日前中国量子物质科学协同创新中心的江颖课题组和王恩哥课题组合作,在水科学领域取得重大突破,在国际上首次实现了水分子的亚分子级分辨成像,使得解析水的氢键网络构型成为可能.(图a是实验器件示意图,图b是拍摄到的图片的一部分,图c是图b所对应的结构示意图)下列有关说法不正确的是( )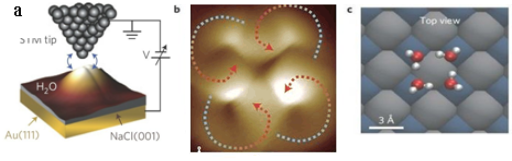
| A. | 图a所示实验器件中,用氯化钠作为绝缘薄膜层,是因为氯化钠晶体不导电 | |
| B. | 图b是表示一个H2O分子内部的氢键和氢氧共价键结构特征示意图 | |
| C. | 水分子间形成氢键使水的熔点和沸点升高 | |
| D. | H2O分子的稳定性很强,是因为分子内氢氧共价键强 |
分析 A、氯化钠固体虽然是离子晶体,但不导电;
B、水分子内部无氢键;
C、分子间存在氢键使物质的熔点和沸点异常的高;
D、稳定性是化学性质,氧的非金属性强,所以氢氧共价键键能大.
解答 解:A、离子不能自由移动,所以氯化钠固体虽然是离子晶体,但不导电,故A正确;
B、水分子内部无氢键,是氢氧极性共价键,故B错误;
C、分子间存在氢键使物质的熔点和沸点异常的高,所以常温下是液体,沸点高达100℃,故C正确;
D、稳定性是化学性质,氧的非金属性强,所以氢氧共价键键能大,故D正确;
故选B.
点评 本题考查考查化学键和氢键的相关知识,综合考查学生的分析能力和基本概念的综合运用能力,为高考常见题型和高频考点,注意相关基础知识的学习,题目难度中等.

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
6.下列四种工业生产:①用海水为原料制镁;②冶炼生铁;③制漂白粉;④工业制备普通玻璃.要用石灰石作为一种原料的( )
| A. | 只有① | B. | 只有①②③ | C. | 只有②③ | D. | 全部 |
7.下列微粒中原子最外层电子数均为8的是( )
| A. | PCl5 | B. | NO2 | C. | NF3 | D. | H2O |
4.下列说法正确的是( )
| A. | 明矾净水过程中不涉及化学变化 | |
| B. | 由同种元素组成的物质一定是纯净物 | |
| C. | 风化、石油分馏和碘的升华都是物理变化 | |
| D. | 为除去蛋白质溶液中少量的NaCl,可以利用渗析的方法 |
11.苯丙酸诺龙是一种兴奋剂,结构简式为有关苯丙酸诺龙的说法不正确的是( )
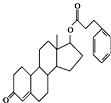

| A. | 含有两种官能团 | B. | 含有脂环 | ||
| C. | 是一种芳香化合物 | D. | 含有酯基 |
1.pH=3的盐酸溶液和pH=5的盐酸溶液等体积混合,则混合溶液的pH是( )
| A. | 4.3 | B. | 5 | C. | 6.3 | D. | 3.3 |
8.下列气体中,可用固体氢氧化钠干燥的是( )
| A. | Cl2 | B. | O2 | C. | SO2 | D. | NO2 |
5.下列离子方程式或化学方程中正确的是( )
| A. | 往NaHSO4溶液中滴加Ba(OH)2至溶液中性:SO42-+2H++Ba2++2OH-═BaSO4↓+2H2O | |
| B. | SO2通入酸性KMnO4溶液,褪色:2MnO4-+4H++5SO2═2Mn2++5SO42-+2H2O | |
| C. | 次氯酸钙溶液中通入过量二氧化碳:Ca2++2ClO-+H2O+CO2═CaCO3?+2HClO | |
| D. | 等物质的量MgCl2、Ba(OH)2和HCl溶液混合:Mg2++3OH-+H+═Mg(OH)2↓+H2O |
6.下列分离混和物的实验计划中不正确的是( )
| A. | 分离乙酸(沸点118℃)与乙酸乙酯(沸点77.1℃)--蒸馏 | |
| B. | 从含有少量NaCl的KNO3溶液中提取KNO3--热水溶解、降温结晶、过滤 | |
| C. | 从水中分离出碘的CCl4溶液--用分液漏斗分液 | |
| D. | 将溴水中的溴转移到有机溶剂中--加入酒精萃取 |