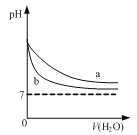
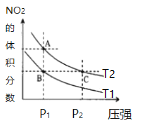
题目内容
【题目】如图是s能级和p能级的原子轨道图。
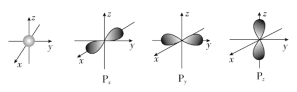
试回答下列问题:
(1)s电子的原子轨道呈________形,每个s能级有________个原子轨道;p电子的原子轨道呈________形,每个p能级有________个原子轨道。
(2)元素X的原子最外层电子排布式为nsnnpn+1,原子中能量最高的是________电子,其电子云在空间有3个互相________(填“垂直”或“平行”)的伸展方向。元素X的名称是________,它的最低价氢化物的电子式是________。
(3)元素Y的原子最外层电子排布式为nsn-1npn+1,Y的元素符号为________,原子的核外电子排布式为______________。
【答案】球 1 哑铃 3 2p轨道 垂直 氮
![]() S [Ne]3s23p4
S [Ne]3s23p4
【解析】
根据图中信息得到s电子、p电子的原子轨道形状和轨道数目;根据元素X的原子最外层电子排布式为nsnnpn+1,得出n值,再进行分析。
(1)s电子的原子轨道呈球形,每个s能级有1个原子轨道;p电子的原子轨道呈哑铃形,每个p能级有3个原子轨道;故答案为:球;1;哑铃;3。
(2)元素X的原子最外层电子排布式为nsnnpn+1,则n =2,因此原子中能量最高的是2p轨道电子,其电子云在空间有3个互相垂直的伸展方向。元素X价电子为2s22p3,其元素名称是氮,它的最低价氢化物为NH3,其电子式是![]() ;故答案为:2p轨道;垂直;氮;
;故答案为:2p轨道;垂直;氮;![]() 。
。
(3)s轨道最多2个电子,因此元素Y的原子最外层电子排布式为3s23p4,则Y为16号元素,其元素符号为S,原子的核外电子排布式为[Ne]3s23p4;故答案为:S;[Ne]3s23p4。

 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案【题目】饮水安全在人们生活中占有极为重要的地位,某研究小组提取三处被污染的水源进行了分析,给出了如下实验信息:其中一处被污染的水源含有A、B两种物质,一处含有C、D两种物质,一处含有E物质。A、B、C、D、E五种常见化合物都是由下表中的离子形成:
阳离子 | K+、Na+、 Cu2+、Al3+ |
阴离子 | SO42-、HCO3-、NO3-、OH- |
为了鉴别上述化合物,分别进行以下实验,其结果如下所示:
①将它们溶于水后,D为蓝色溶液,其他均为无色溶液;
②将E溶液滴入到C溶液中出现白色沉淀,继续滴加,沉淀溶解;
③进行焰色反应,只有B、C为紫色(透过蓝色钴玻璃片);
④在各溶液中加入硝酸钡溶液,再加过量稀硝酸,A中放出无色气体,C、D中产生白色沉淀;
⑤将B、D两溶液混合,未见沉淀或气体生成。
根据上述实验填空:
(1)写出B、D的化学式:B:____________、D:________。
(2)将含1 mol A的溶液与含1 mol E的溶液反应后蒸干,仅得到一种化合物,该化合物为____________。
(3)写出实验②发生反应的离子方程式:___________________、_________________。
(4)C常用作净水剂,用离子方程式表示其净水原理:_________________________。