题目内容
【题目】下列金属防腐的措施中,使用外加电流的阴极保护法的是( )
A. 水中的钢闸门连接电源的负极 B. 金属护栏表面涂漆
C. 汽水底盘喷涂高分子膜 D. 地下钢管连接镁块
【答案】A
【解析】
A.水中的钢闸门连接电源负极,阴极上得电子被保护,所以属于使用外加电流的阴极保护法,故A正确;B.对金属护栏涂油漆使金属和空气、水等物质隔离而防止生锈,没有连接外加电源,故B错误;C.汽车底盘喷涂高分子膜阻止了铁与空气、水的接触,从而防止金属铁防锈,没有连接外加电源,故C错误;D.镁的活泼性大于铁,用牺牲镁块的方法来保护地下钢管而防止铁被腐蚀,属于牺牲阳极的阴极保护法,没有连接外加电源,故D错误;故选A。

【题目】[化学-选修3:物质结构与性质]
铁氧体是一种磁性材料,具有广泛的应用。 -
(1)基态铁原子的核外电子排布式为[Ar]_______。
(2)工业制备铁氧体常使用水解法,制备时常加入尿素[CO(NH2)2 ]、醋酸钠等碱性物质。尿素分子中四种不同元素的电负性由大至小的顺序是____________;醋酸钠中碳原子的杂化类型是_________。
(3)工业制备铁氧体也可使用沉淀法,制备时常加入氨(NH3)、联氨(N2H4)等弱碱。比较下表中氨(NH3)、联氨(N2H4)的熔沸点,解释其高低的主要原因________。
N2H4 | NH3 | |
熔点/℃ | 2 | -77.8 |
沸点/℃ | 113.5 | -33.5 |
(4)下图是从铁氧体离子晶体Fe3O4中,取出的能体现其晶体结构的一个立方体,则晶体中的氧离子是否构成了面心立方最密堆积______(填“是”或“否”),该立方体是不是Fe3O4的晶胞______(填“是”或“否”),立方体中三价铁离子处于氧离子围成的_____空隙(填空间结构)。
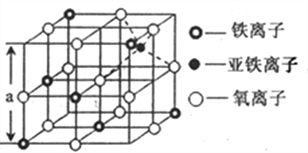
(5)解释该Fe3O4晶体能导电的原因________,根据上图计算Fe3O4晶体的密度_____gcm-3。 (图中a=0.42nm,计算结果保留两位有效数字)