题目内容
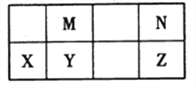
【题目】下表为元素周期表中短周期的一部分,其中Y元素的原子序数为M与N元素原子序数之和。下列说法正确的是
A. 氢化物的稳定性:N >Z,是因为其氢化物分子可形成氢键
B. 元素的非金属性:M > Y,是因为单质M能与YN2反应生成单质Y
C. 熔沸点:YN2>MN2,是因为YN2的分子间作用力强
D. 简单离子的半径:N >X,是因为它们具有相同的电子层结构且X的核电荷数更大
【答案】D
【解析】M、N为第二周期元素,设Y的最外层电子数为x,则M的电子总数为2+x,Y为10+x,N为4+x,根据Y元素的原子序数为M与N元素原子序数之和,则x=4,可知:M为C、N为O、X为Al、Z为S;A.O的非金属性比S强,则氢化物的稳定性是H2O >H2S,与水分子间有氢键无关,故A错误;B.元素的非金属性C> Si,是碳的得电子能力比Si强,故B错误;C.SiO2是原子晶体,而CO2是分子晶体,则熔沸点SiO2>CO2,故C错误;D.O2- 与Al3+具有相同的电子层结构且O的核电荷数更大,则离子半径O2- >Al3+,故D正确;答案为D。

练习册系列答案
相关题目