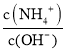��Ŀ����
����Ŀ������������Ҫ�ɷ���![]() ����
����![]() ��
��![]() ��MgO�����ʣ�����ȡ���ֹ���Ʒ���������£�
��MgO�����ʣ�����ȡ���ֹ���Ʒ���������£�

��ش��������⣺
��1�����̼������������Al3+�ķ���ʽΪ_________.
��2�������Ҽ����ռ������SiO32-�����ӷ���ʽΪ________.
��3����֤��ҺB��![]() ����ȡ������Һ������________�����Լ����ƣ���
����ȡ������Һ������________�����Լ����ƣ���
��4����ҺE��K�����ʵ���Ҫ�ɷ���________(�ѧʽ)��д������Һ��һ����;________
��5����֪298Kʱ��![]() ���ݶȻ�����
���ݶȻ�����![]() =5.6��
=5.6��![]() ,ȡ��������ҺB,����һ�������ռ�ﵽ������Һƽ�⣬���PH=13.00������¶��²�������Һ�е�
,ȡ��������ҺB,����һ�������ռ�ﵽ������Һƽ�⣬���PH=13.00������¶��²�������Һ�е�![]() =_______.
=_______.
���𰸡�Al2O3+ 6H��=2Al3��+3H2O SiO2+ 2OH��=SiO32��+ H2O ���軯�أ���������ء�������Һ�Ⱥ����𰸣� NaHCO3 �ƴ���������ͷ۵Ⱥ����� 5.6��10-10mol/L
��������
��1����HCl��Ӧ����Al3����ӦΪ��������Al2O3��Al2O3�����ᷴӦ�����ӷ���ʽΪ��Al2O3+ 6H��=2Al3��+3H2O��
�ʴ�ΪAl2O3+ 6H��=2Al3��+3H2O��
��2��SiO2��������NaOH������Na2SiO3�����ӷ���ʽΪ��SiO2+ 2OH��=SiO32��+ H2O��
�ʴ�ΪSiO2+ 2OH��=SiO32��+ H2O��
��3������Fe3����������Ӧ�ܶ࣬����KSCN��Ѫ��ɫ���뱽������ɫ����OH���Ժ��ɫ�����ȡ�
�ʴ�Ϊ���軯�أ���������ء�������Һ�Ⱥ����𰸣���
��4������E��Kʱ��CO2���ǹ����ģ���Ӧ����NaHCO3���������ƴ���������ͷۣ�
�ʴ�ΪNaHCO3���ƴ���������ͷ۵Ⱥ����𰸣�
��5��pH=13.00��c(OH-)=0.1mol/L������![]() ����
����![]() =5.6��10-12/(0.1)2=5.6��10-10��
=5.6��10-12/(0.1)2=5.6��10-10��
�ʴ�Ϊ5.6��10-10mol/L��

 �¿α�����Ķ�ѵ��ϵ�д�
�¿α�����Ķ�ѵ��ϵ�д� ������������Ӧ����ϵ�д�
������������Ӧ����ϵ�д�