��Ŀ����
����Ŀ����������Ũ�Ⱦ�Ϊ0.5 mol��L-1��������Һ����Na2CO3��Һ ��NaHCO3��Һ ��HCl��Һ �ܰ�ˮ
��1��������Һ�У����ʿɷ���ˮ�����_______________������ţ���
��2�������������������Ʒ�Ӧ�����ܺ����ᷴӦ����Һ�У�����Ũ���ɴ�С��˳��Ϊ_____��
��3������м��������Ȼ�粒��壬��ʱ��Һ��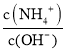 ��ֵ____________ ������������������С����������������
��ֵ____________ ������������������С����������������
��4�������ۺܻ͢�Ϻ���Һǡ�ó����ԣ�����ǰ�۵����________�ܵ��������������������С��������������������ʱ��Һ������Ũ���ɴ�С��˳����_____________��
��5��ȡ10 mL�ۣ���ˮϡ�͵�500 mL�����ʱ��Һ����ˮ�������c(H��)��________��
���𰸡��٢� c(Na+)>c (HCO3-)>c (OH-)>c (H+)>c (CO32-) ���� С�� c(NH4+)=c(Cl-)>c(OH-)=c(H+) 10��12 mol��L-1
��������
(1)���������ӵ����ܷ���ˮ�⣻
(2)�⼸�������У��ܺ�ǿ�ǿ�ᷴӦ������Ϊ�������ʽ�Σ�Ϊ̼�����ƣ�HCO3-����̶�С��ˮ��̶ȣ�����Һ�ʼ��ԣ�ˮҲ�ܵ���������Ӻ����������ӣ��ݴ�����
(3)��ˮ�м����Ȼ������һˮ�ϰ��ĵ��룻
(4)�Ȼ��Ϊǿ�������Σ�����Һ�����ԣ�Ҫʹ����Ͱ�ˮ��Һ�����ԣ���ˮӦ������������ϵ���غ��ж�����Ũ�ȴ�С��
(5)ȡ10mL��Һ��HCl��Һ����ˮϡ�͵�500mL����ҺŨ��Ϊԭ����![]() ��Ϊ0.01mol/L�����ˮ�����ӻ�����������
��Ϊ0.01mol/L�����ˮ�����ӻ�����������
(1)���������ӵ����ܷ���ˮ�⣬̼���ƺ�̼�����ƶ��Ǻ��������ӵ��Σ��ܷ���ˮ�⣬�ʴ�Ϊ�٢ڣ�
(2)�⼸�������У��ܺ�ǿ�ǿ�ᷴӦ��������̼�����ƣ�HCO3-ˮ��̶ȴ��ڵ���̶ȣ����̶ȶ���С����Һ�ʼ��ԣ���Һ��HCO3-��ˮ���������������ӣ�����Һ������Ũ�ȴ�С˳����c(Na+)��c(HCO3-)��c(OH-)��c(H+)��c(CO32-)���ʴ�Ϊc(Na+)��c(HCO3-)��c(OH-)��c(H+)��c(CO32-)��
(3)��ˮ�м����Ȼ�泥���Һ��笠�����Ũ����������һˮ�ϰ����룬����������Ũ�ȼ�С������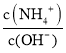 ��ֵ���ʴ�Ϊ����
��ֵ���ʴ�Ϊ����
(4)�Ȼ��Ϊǿ�������Σ�����Һ�����ԣ�Ҫʹ����Ͱ�ˮ��Һ��Ӧ�����ԣ���ˮӦ������������Һ�����ԣ���c(OH-)=c(H+)�����ݵ���غ��c(Cl-)=c(NH4+)��������Һ��ˮ�ĵ���̶Ⱥ�С����������Ũ�ȴ�С˳����c(Cl-)=c(NH4+)��c(OH-)=c(H+)���ʴ�ΪС�ڣ�c(Cl-)=c(NH4+)��c(OH-)=c(H+)��
(5)ȡ10mL��Һ�ۣ���ˮϡ�͵�500mL����ҺŨ��Ϊԭ����![]() ��c(HCl)=0.5mol/L��
��c(HCl)=0.5mol/L��![]() =0.01mol/L����Kw=c(OH-)c(H+)��֪��c(OH-)=10-12 molL-1�����ʱ��Һ����ˮ�������c(H+)=10-12 molL-1���ʴ�Ϊ10-12 molL-1��
=0.01mol/L����Kw=c(OH-)c(H+)��֪��c(OH-)=10-12 molL-1�����ʱ��Һ����ˮ�������c(H+)=10-12 molL-1���ʴ�Ϊ10-12 molL-1��

 �Ƹ������������ϵ�д�
�Ƹ������������ϵ�д�







