题目内容
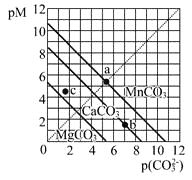
【题目】某温度T1时,Ag2SO4在水中的沉淀溶解曲线如图实线所示。下列说法正确的是( )

A. T1时,Ag2SO4的溶度积常数(Ksp)为1×10-3
B. T1时,0.02 mol/L的AgNO3溶液与0.2 mol/L的Na2SO4溶液等体积混合不会生成沉淀
C. b点表示T1时Ag2SO4的饱和溶液,稀释时可以使溶液由b点变到a点
D. 仅通过降温的方法,可以使T2时的饱和溶液从c点变到T1时b点
【答案】B
【解析】选取图中的b点,得到Ksp=(2×10-2)2×5×10-2=2×10-5,选项A错误。混合的瞬间溶液为:0.01 mol/L的AgNO3和0.1 mol/L的Na2SO4混合溶液(注意溶液体积是原来的2倍),所以QC=(0.01)2×0.1=1×10-5<Ksp=2×10-5,所以不会出沉淀。选项B正确。对于硫酸银的饱和溶液,加水稀释应该是硫酸根和银离子浓度都减小,而从b到a,银离子的浓度不变,所以选项C是错误的。降温,硫酸银的溶解度下降,硫酸银从溶液中析出,所以是硫酸根和银离子浓度都减小,而从c到b,硫酸根离子的浓度不变,所以选项D是错误的。

练习册系列答案
 一线名师权威作业本系列答案
一线名师权威作业本系列答案
相关题目