题目内容
【题目】重铬酸钾(K2Cr2O7)常用作有机合成的氧化剂和催化剂等。由含铬废液(主要含Cr3+、Fe3+、K+、SO42-等)制备K2Cr2O7的流程如图所示。

已知:I.在酸性条件下,H2O2能将Cr2O72-还原为Cr3+
II.相关金属离子形成氢氧化物沉淀的pH范围:
金属离子 | 开始沉淀的pH | 沉淀完全的pH |
Cr3+ | 4.9 | 6.8 |
Fe3+ | 1.5 | 2.8 |
回答下列问题:
(1)滤渣②的成分是________________。
(2)写出“氧化”步骤中反应的化学方程式________________。
(3)“加热”操作的目的是________________。
(4)根据平衡移动原理解释酸化至pH=1的目的是________________(用离子方程式和适当文字说明)。
(5)通过下列实验可测定产品中K2Cr2O7(M=294g/mol)的纯度:称取重铬酸钾试样1.470g,用100mL容量瓶配制成溶液。移取25.00mL溶液于碘量瓶中,加入适量稀硫酸和足量碘化钾(Cr2O72-的还原产物为Cr3+),放于暗处5min。然后加入一定量的水,加入淀粉指示剂,用0.1500mol/LNa2S2O3标准溶液滴定,共消耗标准液36.00mL。滴定时发生的反应的离子方程式为:I2+2S2O32-=2I-+S4O62-。则所测定产品中K2Cr2O7的纯度为________________。
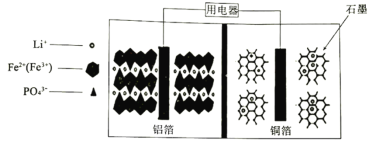
(6)在K2Cr2O7存在下,可利用微生物电化学技术实现含苯酚废水的有效处理,其工作原理如图所示。

①负极的电极反应式为________________;
②一段时间后,中间室NaCl溶液的浓度________________(填“增大”“减小”或“不变”)。
【答案】Fe(OH)3(或氢氧化铁) 2Cr(OH)3+3H2O2+4KOH=2K2CrO4+8H2O 除去过量的H2O2 2CrO42-+2H+Cr2O72-+H2O,酸化至pH=1,促进该反应平衡正向移动,实现CrO42-转化为Cr2O72- 72.00%(72%或72.0%也可) C6H5OH+11H2O﹣28e-=6CO2↑+28H+ 减小
【解析】
含铬废液(主要含Cr3+、Fe3+、K+、SO42-等)制备K2Cr2O7的流程:废液与足量KOH反应生成沉淀Cr(OH)3、Fe(OH)3,过滤得到滤渣①Cr(OH)3、Fe(OH)3混合物,除去K+、SO42-等离子,碱性条件下在滤渣中加入过氧化氢氧化Cr(OH)3生成K2CrO4,过滤除去Fe(OH)3,则滤渣②为Fe(OH)3,得到K2CrO4滤液②,加热除去过量过氧化氢,防止后续加酸时H2O2能将Cr2O72-还原为Cr3+,加酸调pH=1,使K2CrO4溶液转化为K2Cr2O7溶液,蒸发结晶得到K2Cr2O7晶体,以此解答。
(1)根据分析,过滤得到滤渣①Cr(OH)3、Fe(OH)3混合物,“氧化”步骤中加入过氧化氢氧化Cr(OH)3生成K2CrO4,过滤除去Fe(OH)3,滤渣②的成分是Fe(OH)3(或氢氧化铁);
(2)“氧化”步骤中,碱性条件下,过氧化氢氧化Cr(OH)3生成K2CrO4溶液,结合电子守恒、原子守恒,化学方程式为2Cr(OH)3+3H2O2+4KOH=2K2CrO4+8H2O;
(3)结合已知信息,在酸性条件下,H2O2能将Cr2O72-还原为Cr3+,为防止后续“酸化”步骤中H2O2将Cr2O72-还原为Cr3+而混入杂质,所以酸化前必须除去H2O2,并且H2O2不稳定易分解,通过加热可除去;
(4)由于酸性条件下,CrO42-可转化为Cr2O72-,发生反应为:2CrO42-+2H+Cr2O72-+H2O,酸化至pH=1,促进该反应平衡正向移动,实现CrO42-转化为Cr2O72-;
(5)根据实验步骤可知,用碘化钾将Cr2O72还原成Cr3+,根据电子得失守恒有关系式Cr2O723I2,再用Na2S2O3标准溶液滴定(I2+2S2O32=2I+S4O62),所以有关系式Cr2O723I26S2O32,Na2S2O3的物质的量为0.1500mol/L×0.036L=5.4×103mol,所以样品中K2Cr2O7的物质的量![]() ×5.4×103mol×
×5.4×103mol×![]() =3.6×103mol,样品中K2Cr2O7的纯度为
=3.6×103mol,样品中K2Cr2O7的纯度为![]() ×100%=72.00%;
×100%=72.00%;
(6)①根据图示,C6H5OH转化为CO2,则苯酚发生氧化反应、作负极,结合电子守恒和电荷守恒有负极的电极反应式为C6H5OH+11H2O﹣28e-=6CO2↑+28H+;
②由于电解质NaCl溶液被阳离子交换膜和阴离子交换膜隔离,使Na+和Cl-不能定向移动,所以电池工作时,负极生成的H+透过阳离子交换膜加入NaCl溶液中,正极生成的OH-透过阴离子交换膜进入NaCl溶液中与H+反应生成水,使NaCl溶液浓度减小。

 阅读快车系列答案
阅读快车系列答案