题目内容
【题目】2019年诺贝尔化学奖授子对锂离子电池研究做出贡献的三位科学家。高能磷酸铁锂电池多应用于公共交通,内部结构如图,电池中间是聚合物的隔膜。电池在充电过程中,LiFePO4逐渐脱离出锂离子形成FePO4。下列叙述不正确的是
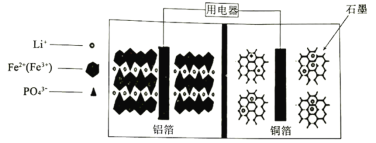
A.放电时Li+通过隔膜移向正极B.放电时正极反应式为:FePO4+Li++e-=LiFePO4
C.充电时铜箔连接电源负极D.充电时,每转移1mol电子,石墨增重12g
【答案】D
【解析】
电池在充电过程中为电解池,LiFePO4逐渐脱离出锂离子形成FePO4,Fe元素由+2价变为+3价,化合价升高,失电子,发生氧化反应,所在铝电极为阳极,则放电(原电池)时,FePO4所在铝电极为正极,发生得电子的还原反应,正极电极反应式为FePO4+Li++e-═LiFePO4,铜电极为负极,电极反应为:LixCn-xe-═xLi++nC;充电时为电解池,原电池的正、负极分别与电源的正、负极相接、作电解池的阳极、阴极,阳、阴极电极反应与原电池正、负极的恰好相反,电解质中阳离子移向阴极、阴离子移向阳极,据此分析解答。
A.放电时为原电池,原电池中,阳离子向正极移动,根据分析,铝电极为正极,Li+通过隔膜移向正极,故A正确;
B.根据分析,放电时正极反应式为:FePO4+Li++e-=LiFePO4,故B正确;
C.结合分析,充电时为电解池,原电池的正、负极分别与电源的正、负极相接,作电解池的阳极、阴极,铜箔为原电池的负极,应与电源负极连接,故C正确;
D.充电时,阴极反应式为nC+xLi++xe=LixCn,则通过1mol电子石墨电极增加1molLi+,增重质量为7g,故D错误;
答案选D。

 阅读快车系列答案
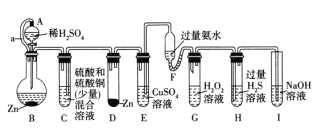
阅读快车系列答案【题目】下列实验操作中,根据实验现象得出的结论正确的是
选项 | 操作 | 现象 | 结论 |
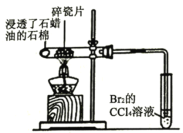
A |
| Br2的CCl4溶液褪色 | 石蜡油分解产生乙烯气体 |
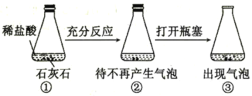
B |
| ③中出现气泡 | 可以用平衡移动原理解释 |
C |
| ①中出现白色沉淀 ②中出现红褐色沉淀 | Ksp[Fe(OH)3]<Ksp[Mg(OH)2] |
D |
| 淀粉碘化钾溶液变蓝 | b为直流电源负极 |
A.AB.BC.CD.D
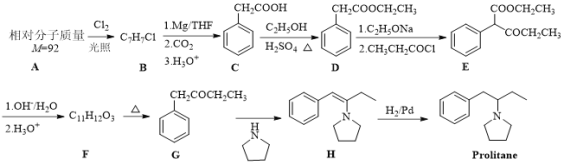
【题目】重铬酸钾(K2Cr2O7)常用作有机合成的氧化剂和催化剂等。由含铬废液(主要含Cr3+、Fe3+、K+、SO42-等)制备K2Cr2O7的流程如图所示。

已知:I.在酸性条件下,H2O2能将Cr2O72-还原为Cr3+
II.相关金属离子形成氢氧化物沉淀的pH范围:
金属离子 | 开始沉淀的pH | 沉淀完全的pH |
Cr3+ | 4.9 | 6.8 |
Fe3+ | 1.5 | 2.8 |
回答下列问题:
(1)滤渣②的成分是________________。
(2)写出“氧化”步骤中反应的化学方程式________________。
(3)“加热”操作的目的是________________。
(4)根据平衡移动原理解释酸化至pH=1的目的是________________(用离子方程式和适当文字说明)。
(5)通过下列实验可测定产品中K2Cr2O7(M=294g/mol)的纯度:称取重铬酸钾试样1.470g,用100mL容量瓶配制成溶液。移取25.00mL溶液于碘量瓶中,加入适量稀硫酸和足量碘化钾(Cr2O72-的还原产物为Cr3+),放于暗处5min。然后加入一定量的水,加入淀粉指示剂,用0.1500mol/LNa2S2O3标准溶液滴定,共消耗标准液36.00mL。滴定时发生的反应的离子方程式为:I2+2S2O32-=2I-+S4O62-。则所测定产品中K2Cr2O7的纯度为________________。
(6)在K2Cr2O7存在下,可利用微生物电化学技术实现含苯酚废水的有效处理,其工作原理如图所示。
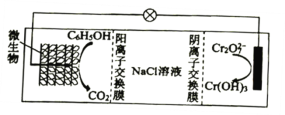
①负极的电极反应式为________________;
②一段时间后,中间室NaCl溶液的浓度________________(填“增大”“减小”或“不变”)。