题目内容
下列说法错误的是
| A.化学反应的速率越大,化学反应的限度越大 |
| B.化学反应中既有物质变化,又有能量变化 |
| C.化学反应的实质是旧键的断裂,新键的形成 |
| D.可逆反应达到化学平衡状态,反应依然在进行 |
A
试题分析:A、反应速率快慢与反应限度无关系,A不正确;B、化学反应的特征就是有新物质生成,又伴随能量的变化,由此化学反应中既有物质变化,又有能量变化,B正确;C、化学反应的实质是旧键的断裂,新键的形成,C正确;D、在一定条件下,当可逆反应中正反应速率和逆反应速率相等时(但不为0),各种物质的浓度或含量均不再发生变化的状态,是化学平衡状态,所以可逆反应达到化学平衡状态,反应依然在进行,D正确,答案选A。

练习册系列答案
相关题目
 H2(g)+CO2(g) △H=-41.2kJ/mol ,制备CO2与H2的混合气体,并进一步研究CO2与H2以不同的体积比混合时在合适条件下的反应产物应用。
H2(g)+CO2(g) △H=-41.2kJ/mol ,制备CO2与H2的混合气体,并进一步研究CO2与H2以不同的体积比混合时在合适条件下的反应产物应用。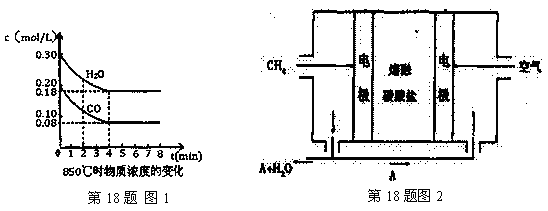
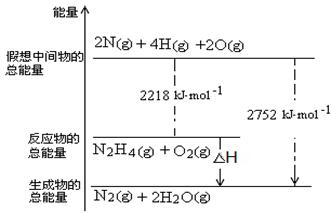
 2NH3(g)ΔH=-92.4 kJ·mol-1
2NH3(g)ΔH=-92.4 kJ·mol-1
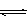 CH3OH(g)
CH3OH(g)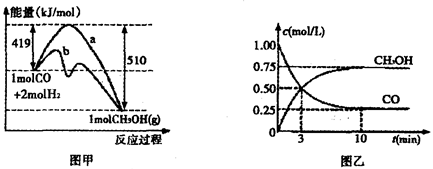
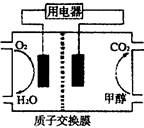
 CO(g)+H2(g);ΔH= 。(用含ΔH1、ΔH2的代数式表示)
CO(g)+H2(g);ΔH= 。(用含ΔH1、ΔH2的代数式表示)