题目内容
【题目】根据核外电子的排布特点推断元素的性质:
(1)A元素基态原子的最外层有3个未成对电子,次外层有2个电子,其基态原子的电子排布图为_____,在周期表中位于___区。
(2) B元素基态原子的M层全充满,N层没有成对电子且只有一个未成对电子,B的基态原子的价层电子排布式为_______。
(3)请利用电子排布的相关知识稳定性:Fe3+______Fe2+(填>或< ),原因___________,第一电离能:Mg____Al(填>或< )原因__________。
(4) 有以下物质:①H2 ②N2 ③CO2 ④N2H4⑤H2O2 ⑥HCN(H—C≡N);只有σ键的是______;既有σ键又有π键的是__________;含有由两个原子的s轨道重叠形成的σ键的是_____;含有由一个原子的s轨道与另一个原子的p轨道重叠形成的σ键的是______;
(5) 通过 (3)的解答,请归纳基态原子核外电子排布除了符合构造原理外,泡利原理、洪特规则外,还有哪些结构稳定__________。
【答案】![]() p 3d104s1 > 正三价铁离子的3d轨道电子数为5,为半充满的稳定状态,二价铁离子3d轨道电子数为6,为不稳定状态 > Mg元素基态原子的3s全充满,为稳定状态,Al元素基态原子的3p能级上只有1个电子,为不稳定状态 ①④⑤ ②③⑥ ① ④⑤ ⑥ 全充满 、半充满 、全空结构
p 3d104s1 > 正三价铁离子的3d轨道电子数为5,为半充满的稳定状态,二价铁离子3d轨道电子数为6,为不稳定状态 > Mg元素基态原子的3s全充满,为稳定状态,Al元素基态原子的3p能级上只有1个电子,为不稳定状态 ①④⑤ ②③⑥ ① ④⑤ ⑥ 全充满 、半充满 、全空结构
【解析】
(1)A元素基态原子的最外层有3个未成对电子,次外层有2个电子,说明A原子有两个能层,其基态原子的电子排布1s22s22p3,其基态原子的电子排布图为![]() ,价电子的电子排布2s22p3,在周期表中位于p区。
,价电子的电子排布2s22p3,在周期表中位于p区。
(2) B元素基态原子的M层全充满,3d能层是全充满,N层没有成对电子且只有一个未成对电子,即4s能层上只有1个电子,B的基态原子的价层电子排布式为3d104s1。
(3)根据电子排布的相关知识得:稳定性:Fe3+>Fe2+,原因正三价铁离子的3d轨道为半充满,3d轨道电子数为5,为稳定状态,二价铁离子3d轨道电子数为6,为不稳定状态;
第一电离能:Mg>Al,Mg元素基态原子的3s全充满,为稳定状态,Al元素基态原子的3p能级上只有1个电子,为不稳定状态。
(4) 有以下物质:①H2 ②N2 ③CO2 ④N2H4⑤H2O2 ⑥HCN(H—C≡N);只有σ键的是①④⑤;既有σ键又有π键的是②③⑥;含有由两个原子的s轨道重叠形成的σ键的是①;含有由一个原子的s轨道与另一个原子的p轨道重叠形成的σ键的是④⑤ ⑥;
(5) 通过 (3)的解答,基态原子核外电子排布除了符合构造原理外,泡利原理、洪特规则外,还有全充满 、半充满 、全空结构稳定。

 优化作业上海科技文献出版社系列答案
优化作业上海科技文献出版社系列答案【题目】对甲烷和CO2的高效利用不仅能缓解大气变暖,而且对日益枯竭的石油资源也有一定的补充作用,甲烷临氧耦合CO2重整反应有:
反应(i):2CH4(g)+O2(g)![]() 2CO(g)+4H2(g) △H=-71.4kJmol-1
2CO(g)+4H2(g) △H=-71.4kJmol-1
反应(ii):CH4(g)+CO2(g)![]() 2CO(g)+2H2(g) △H=+247.0kJmol-1
2CO(g)+2H2(g) △H=+247.0kJmol-1
(1)写出表示CO燃烧热的热化学方程式:_____。
(2)在两个体积均为2L的恒容密闭容器中,起始时按表中相应的量加入物质,在相同温度下进行反应(ii):CH4(g)+CO2(g)![]() 2CO(g)+2H2(g)(不发生其它反应),CO2的平衡转化率如下表所示:
2CO(g)+2H2(g)(不发生其它反应),CO2的平衡转化率如下表所示:
起始物质的量(n)/mol | CO2的平衡转化率 | ||||
CH4 | CO2 | CO | H2 | ||
Ⅰ | 0.1 | 0.1 | 0 | 0 | 50% |
Ⅱ | 0.1 | 0.1 | 0.2 | 0.2 | / |
①下列能说明反应达到平衡状态是_____。
A.v正(CH4)=2v逆(CO)
B.容器内各物质的浓度满足c(CH4)·c(CO2)=c2(CO)·c2(H2)
C.容器内混合气体的总压强不再变化
D.容器内混合气体密度保持不变
②若容器Ⅰ内反应从开始到平衡所用的时间为tmin,则tmin内该反应的平均反应速率为:v(H2)=____(用含t的表达式表示)。
③达到平衡时,容器Ⅰ、Ⅱ内CO的物质的量的关系满足:2n(CO)Ⅰ___n(CO)Ⅱ(填“>”、“=”或“<”)。
(3)将CH4(g)和O2(g)以物质的量比为4:3充入盛有催化剂的恒容密闭容器内,发生上述反应(i):2CH4(g)+O2(g)![]() 2CO(g)+4H2(g)
2CO(g)+4H2(g)

①T2℃时,CO体积分数最大的原因是____。
②若T2℃时,容器内起始压强为P0,平衡时CO的体积分数为20%,则反应的平衡常数KP=___(用平衡分压强代替平衡浓度计算,分压=总压×物质的量分数)。
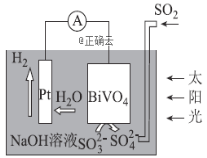
(4)2016年我国科研人员根据反应Na+CO2→Na2CO3+C(未配平)研制出一种室温“可呼吸”Na-CO2电池。放电时该电池“吸入”CO2,充电时“呼出”CO2。其放电时的工作原理如图所示,已知吸收的全部CO2中,有![]() 转化为Na2CO3固体沉积在多壁碳纳米管(MWCNT)电极表面,写出放电时正极的电极反应式:___。
转化为Na2CO3固体沉积在多壁碳纳米管(MWCNT)电极表面,写出放电时正极的电极反应式:___。