题目内容
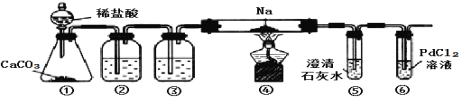
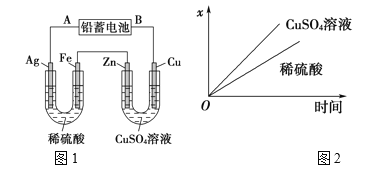
【题目】已知铅蓄电池的工作原理为Pb(s)+PbO2(s)+2H2SO4(aq)![]() 2PbSO4(s)+2H2O(l),现用如图1装置进行电解(电解液足量),测得当铅蓄电池中转移0.4mol电子时,铁电极的质量减少11.2g。请回答下列问题:
2PbSO4(s)+2H2O(l),现用如图1装置进行电解(电解液足量),测得当铅蓄电池中转移0.4mol电子时,铁电极的质量减少11.2g。请回答下列问题:
(1)A是铅蓄电池的________极,铅蓄电池正极反应式为:______。
(2)Ag电极的电极反应式是______,该电极的电极产物共________g。
(3)Cu电极的电极反应式是________,CuSO4溶液的浓度_______(填“减小”“增大”或“不变”)。
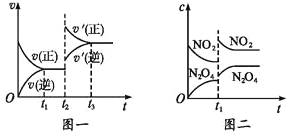
(4)如图2表示电解进行过程中某个量(纵坐标x)随时间的变化曲线,则x表示_______。
a.各U形管中产生的气体的体积
b.各U形管中阳极质量的减少量
c.各U形管中阴极质量的增加量
【答案】负 PbO2+4H++SO42-+2e-===PbSO4+2H2O 2H++2e-===H2↑ 0.4 Cu-2e-===Cu2+ 不变 b
【解析】
已知铅蓄电池中转移0.4mol电子时,铁电极的质量减少11.2g,则稀硫酸电解池中Fe为阳极,硫酸铜电解池中Cu为阳极,铅蓄电池B为正极,A为负极;
(1)分析可知,A是铅蓄电池的负极;铅蓄电池正极二氧化铅得电子,与硫酸反应生成硫酸铅和水,电极反应式为PbO2+4H++SO42-+2e-=PbSO4+2H2O;
(2)Ag电极为电解池的阴极,氢离子得电子生成氢气,电极反应式为2H++2e-=H2↑;转移0.4mol电子时,生成0.2mol氢气,即0.4g;
(3)Cu电极为阳极,铜失电子生成铜离子,电极反应式为Cu-2e-=Cu2+;溶液中的铜离子在阴极得电子生成铜,则溶液中的铜离子浓度不变;
(4)a.硫酸铜溶液中无气体生成,与图象不符,a错误;
b.各U形管中阳极分别为Fe、Cu,随反应时间的增大,质量逐渐减少,符合图象,b正确;
c.稀硫酸电解池中阴极产生氢气,阴极的质量不变,与图象不符,c错误;
答案为b。