题目内容
无机非金属材料、金属材料和有机高分子材料并称为三大材料,是发展高新技术的基石,在未来科技发展中发挥着重要的作用。
(1)新型材料α-Fe粉具有超强的磁性能,用作高密度磁记录的介质以及高效催化剂等。将5.60 g α-Fe粉与一定量水蒸气在高温下反应一定时间后冷却,其质量变为6.88 g。
①产生的氢气的体积为_________mL(标准状况下)。
②将冷却后的固体物质放入足量FeCl3溶液中充分反应(已知Fe3O4不溶于FeCl3溶液),计算最多消耗FeCl3的物质的量 mol。
(2)Nierite是一种高熔点高硬度的陶瓷材料。Nierite的摩尔质量为140 g/mol,其中硅元素的质量分数为60%。已知1 mol NH3与足量的化合物T充分反应后可得到35 g Nierite与3 mol HCl气体。
Nierite的化学式为___________。T的化学式为____________。
(3)K金是常见的贵金属材料,除黄金外,还含有银、铜中的一种或两种金属。为测定某18K金样品的组成,将2.832 g样品粉碎后投入足量的浓硝酸中,充分溶解后,收集到NO2和N2O4的混合气体224 mL(折算至标准状况,下同),将该混合气体与84 mL O2混合后缓缓通入水中,恰好被完全吸收。
①混合气体的平均摩尔质量为______________。
②填写该18K金的成分表(精确至0.01%,若不含该金属则填0)。
| 18K金成分 | Au | Ag | Cu |
| 含量(质量分数) | 75.00% | _________ | _________ |
(1)①1792(2分);②0.08 2分,
(2)Si3N4(2分);SiCl4(2分)
(3)①69 g/mol(2分);
②Ag:11.44%;Cu:13.56%(4分)
解析试题分析:(1)铁与水蒸气反应3Fe+4H2O=Fe3O4+4H2,物质增加的质量为氧元素,n(H2)=n(O)=(6.88-5.60)÷16=0.08mol v(H2)=0.08×22.4×1000=1792mL(2)n(Fe)=5.6÷56=0.1mol,n(Fe3O4)=n(O)÷4=0.02mol,故固体中剩余的铁单质为0.04mol,消耗FeCl3的量为n(FeCl3)=2n(Fe)=0.08mol
(2)Nierite确定有硅元素和氮元素,化学式中硅元素原子个数为140×60%÷28=3,氮原子个数为140×40%÷14=4,故化学式为Si3N4;根据原子守恒可以得出T的化学式为SiCl4;
(3)假设气体全为NO2,则有4NO2+H2O+O2=4HNO3,m(NO2)=84×10-3÷22.4×46×4=0.69g,气体的质量不变,则混合气体的平均摩尔质量为0.69÷(224×10-3÷22.4)="69" g/mol
设K金中含有铜银两种金属,则根据质量关系列等式为64n(Cu)+108n(Ag)=2.832×25%
金不溶于硝酸,铜银溶于硝酸,根据电子守恒得出等式为2n(Cu)+n(Ag)=84×10-3÷22.4×4(氧气得到的电子),二者联立解得n(Cu)=0.006mol,n(Ag)=0.003mol,百分含量分别为Ag:11.44%;Cu:13.56%。
考点:考查化学计算有关问题。

有同学研究从矿石开始到产出钢铁的工艺流程。
(1)将6.62g铁矿石样品投入足量的盐酸中完全溶解后过滤,滤渣中不含铁元素。在滤液中加过量的NaOH溶液,充分反应,过滤、洗涤、灼烧得4.80g Fe2O3。求该铁矿石含铁的质量分数。
(2)现以该铁矿石为原料炼铁,若生产过程中铁元素损失4%,计算每生产1.00吨生铁(含铁96%),至少需要这种铁矿石多少吨?(保留两位小数)
(3)取某钢样粉末28.12g(假设只含Fe和C),在氧气流中充分反应,得到CO2气体224mL(标准状况)。计算此钢样粉末中铁和碳的物质的量之比。
(4)再取三份不同质量的上述钢样粉末,分别加到100mL相同浓度的H2SO4溶液中,充分反应后,测得的实验数据如下表所示:
| 实验序号 | Ⅰ | Ⅱ | Ⅲ |
| 加入钢样粉末的质量/g | 2.812 | 5.624 | 8.436 |
| 生成气体的体积/L(标准状况) | 1.120 | 2.240 | 2.800 |
计算硫酸溶液的物质的量浓度
(5)若在实验Ⅱ中继续加入mg钢样粉末,计算反应结束后剩余的固体质量为多少?(用含m的代数式表示)
用18.4mol/L的浓硫酸稀释成0.92mol/L的稀硫酸100ml,回答下列问题:
(1)
| 应取浓硫酸的体积/ml | 应选用容量瓶的规格/mL | 除容量瓶外还需要的其它仪器 |
| | | |
(2)配制操作可分解成如下几步:
A.向容量瓶中注入少量蒸馏水,检查容量瓶是否漏水
B.用少量蒸馏水洗涤烧杯,将溶液注入容量瓶,并重复操作两次
C.将已冷却的硫酸注入容量瓶中
D.根据计算,用量筒量取一定体积的浓硫酸
E.将浓硫酸沿烧杯壁慢慢注入盛有蒸馏水的小烧杯中,并不断用玻璃棒搅拌
F.盖上容量瓶塞子,振荡,摇匀,装瓶
G.用胶头滴管继续加蒸馏水,使溶液凹面恰好与刻度相切
H.继续往容量瓶中小心地加蒸馏水,使液面接近刻度线
正确的操作顺序是:A____________________________F
(3)下列操作结果,使溶液物质的量浓度偏低的是
A.没有将洗涤液转移到容量瓶中
B.容量瓶洗净后未经干燥处理
C.转移过程中有少量的溶液溅出
D.摇匀后立即观察,发现溶液未达刻度线,没有再用滴管加几滴蒸馏水至刻度线
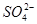 和
和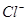 的物质的量浓度(假定在混合液中加入氢氧化钡粉末后体积未改变)。
的物质的量浓度(假定在混合液中加入氢氧化钡粉末后体积未改变)。 Cu3P2+3H2而增重4.96 g;第二支玻璃管反应后质量减轻了5.76 g。
Cu3P2+3H2而增重4.96 g;第二支玻璃管反应后质量减轻了5.76 g。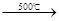 Na2SO4+2HCl↑
Na2SO4+2HCl↑ Na2S+2CO2↑
Na2S+2CO2↑