题目内容
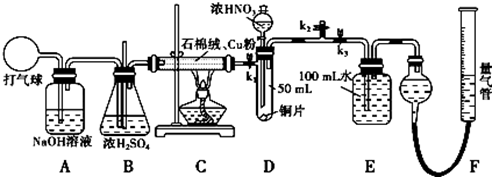
3.红热木炭与浓H2SO4反应的化学方程式是C+2H2SO4(浓)$\frac{\underline{\;\;△\;\;}}{\;}$CO2↑+2SO2↑+2H2O浓硫酸的作用是强氧化剂.按下图装置进行实验,可证明碳和浓硫酸反应放出气体SO2和CO2气体.已知图中4个洗气瓶均装有检测液.现给出4种溶液①品红溶液②酸性高锰酸钾溶液③品红溶液④澄清石灰水.试指出各洗气瓶内所盛液体的作用.①检验二氧化硫②除去二氧化硫③检验二氧化硫是否除尽④检验二氧化碳

分析 C和浓硫酸反应方程式为C+2H2SO4(浓) $\frac{\underline{\;\;△\;\;}}{\;}$CO2↑+2SO2↑+2H2O,该反应中生成CO2、SO2,这两种气体都能使澄清石灰水变浑浊,但二氧化硫具有漂白性、还原性,所以能使品红溶液褪色,能被酸性高锰酸钾氧化,该反应中浓硫酸作氧化剂,以此解答该题.
解答 解:红热木炭与浓H2SO4反应的化学方程式是C+2H2SO4(浓) $\frac{\underline{\;\;△\;\;}}{\;}$CO2↑+2SO2↑+2H2O,反应中S元素化合价降低,浓硫酸起到氧化剂的作用,CO2、SO2这两种气体都能使澄清石灰水变浑浊,但二氧化硫具有漂白性、还原性,所以能使品红溶液褪色,能被酸性高锰酸钾氧化,所以将混合气体通入第一个洗气瓶中检验二氧化硫、通入第二个洗气瓶中除去二氧化硫、通入第三个洗气瓶中排除二氧化硫的存在,第四个洗气瓶检验二氧化碳,
故答案为:C+2H2SO4(浓) $\frac{\underline{\;\;△\;\;}}{\;}$CO2↑+2SO2↑+2H2O;强氧化剂;检验二氧化硫;除去二氧化硫;检验二氧化硫是否除尽;检验二氧化碳.
点评 本题以浓硫酸和碳的反应为载体考查物质的检验,明确物质的性质是解本题关键,根据CO2、SO2这两种气体性质的相似性和差异性设计实验即可,知道常见物质的检验方法,题目难度不大.

练习册系列答案
相关题目
18.下列反应中,能用离子方程式H++OH-═H2O表示的是( )
| A. | Ba(OH)2溶液与稀H2SO4 | B. | NaOH溶液与醋酸 | ||
| C. | Fe(OH)3溶液与稀H2SO4 | D. | Ba(OH)2溶液与稀HNO3 |
12.工业生产硫酸过程中,SO2在接触室中被催化氧化为SO3气体,已知该反应为放热反应.现将2mol SO2、1mol O2充入一密闭容器充分反应后,放出热量98.3kJ,此时测得SO2的转化率为50%,则下列热化学方程式正确的是( )
| A. | 2SO2(g)+O2(g)?2SO3(g)△H=-196.6 kJ•mol-1 | |
| B. | 2SO2(g)+O2(g)?2SO3(g)△H=-98.3 kJ•mol-1 | |
| C. | SO2(g)+$\frac{1}{2}$O2(g)?SO3(g)△H=+98.3 kJ•mol-1 | |
| D. | SO2(g)+$\frac{1}{2}$O2(g)?SO3(g)△H=-196.6 kJ•mol-1 |
 由于Fe(OH)2极易被氧化,所以实验室难用亚铁盐溶液与烧碱反应制得白色纯净的Fe(OH)2沉淀.若用如图所示实验装置可制得纯净的Fe(OH)2沉淀.两极材料分别为石墨和铁.
由于Fe(OH)2极易被氧化,所以实验室难用亚铁盐溶液与烧碱反应制得白色纯净的Fe(OH)2沉淀.若用如图所示实验装置可制得纯净的Fe(OH)2沉淀.两极材料分别为石墨和铁.