题目内容
11.水杨酸环已酯具有花香气味,可作为香精配方.其合成路线如图: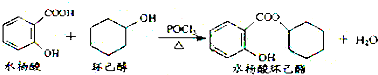
下列说法正确的是( )
| A. | 水杨酸能分别与NaHCO3、Na2CO3溶液反应,且1 mol水杨酸分别消耗NaHCO32mol、Na2CO31mol | |
| B. | 水杨酸、环己醇和水杨酸环己酯均能与FeCl3溶液发生显色反应 | |
| C. | 1 mol水杨酸环己酯在NaOH溶液中水解时,最多消耗3 mol NaOH | |
| D. | 1 mol水杨酸跟足量浓溴水反应时,最多消耗Br2 2 mol |
分析 A.水杨酸中含有羧基和酚羟基,能和碳酸钠反应,酚羟基不能和碳酸氢钠反应;
B.酚羟基能和氯化铁溶液发生显色反应;
C.酚羟基、羧基能和NaOH反应;
D.水杨酸苯环上酚羟基邻对位氢原子能被溴原子取代.
解答 解:A.水杨酸中含有羧基和酚羟基,能和碳酸钠反应,但酚羟基不能和碳酸氢钠反应,故A错误;
B.酚羟基能和氯化铁溶液发生显色反应,环己醇中不含酚羟基,所以不能发生显色反应,故B错误;
C.酚羟基、羧基能和NaOH反应,1 mol水杨酸环己酯在NaOH溶液中水解时,最多生成1mol酚羟基、1mol羧基,所以最多消耗2mol NaOH,故C错误;
D.水杨酸苯环上酚羟基邻对位氢原子能被溴原子取代,所以1 mol水杨酸跟足量浓溴水反应时,最多消耗Br2 2 mol,故D正确;
故选D.
点评 本题考查有机物结构和性质,明确官能团及其性质关系是解本题关键,侧重考查酚、羧酸、酯的性质,注意酚和溴发生取代反应位置,酚羟基和碳酸氢钠不反应,这些都是易错点.

练习册系列答案
相关题目
16.某氢氧燃料电池是用金属铂作电极,以KOH溶液作电解质溶液,从两极分别通入H2和O2.下列对该燃料电池的叙述中正确的是( )
| A. | 负极的电极反应式为:H2-2e-+2OH-═2H2O | |
| B. | H2应从负极通入,发生还原反应 | |
| C. | 标准状况下,通入5.6 L O2并完全反应后,有0.50 mol电子转移 | |
| D. | 放电一段时间后,通入O2的电极附近溶液的pH降低 |
3.如图是酸性氢氧燃料电池构造示意图.关于该电池的说法不正确的是( )
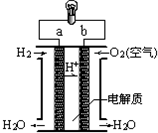

| A. | a极是负极 | |
| B. | 电流由b通过灯泡流向a | |
| C. | 正极的电极反应是:O2+2H2O+4e-═4OH- | |
| D. | 氢氧燃料电池是环保电池 |
20.钾的金属活动性比钠强,根本原因是( )
| A. | 钾的密度比钠的小 | B. | 加热时,钾比钠更易气化 | ||
| C. | 钾与水反应比钠与水反应更剧烈 | D. | 钾原子的电子层比钠原子多一层 |
1.下列说法正确的是( )
| A. | 用红外光谱可鉴别乙醇和二甲醚,用X-射线衍射实验可鉴别玻璃与水晶 | |
| B. | 煤的主要成分是单质碳、苯、二甲苯等,可通过煤的干馏将它们分离 | |
| C. | 聚氯乙烯塑料可制作保鲜膜、一次性食品袋 | |
| D. | 聚乙烯塑料的老化是由于发生了加成反应 |
 .
.